Industri Kontruksi
Menggabungkan Lean Construction dan Kecerdasan Buatan: Revolusi Manajemen Proyek Konstruksi
Dipublikasikan oleh Izura Ramadhani Fauziyah pada 23 April 2025
Dunia konstruksi sedang mengalami revolusi digital yang luar biasa. Di satu sisi, pendekatan Lean Construction (LC) menekankan penghapusan pemborosan dan peningkatan nilai. Di sisi lain, Artificial Intelligence (AI), terutama Machine Learning (ML), menjanjikan prediksi yang akurat, efisiensi otomatisasi, dan pengambilan keputusan berbasis data. Artikel tinjauan sistematik dari Velezmoro-Abanto dan koleganya ini menjadi titik temu penting antara keduanya—mengungkap bagaimana integrasi LC dan AI mengubah wajah manajemen proyek konstruksi (PM).
Dengan menggunakan pendekatan PRISMA, penulis berhasil menyaring 63 artikel kunci dari 43.654 publikasi global untuk mengidentifikasi tren, alat, manfaat, dan tantangan integrasi ini.
Peta Literatur Global: Di Mana Penelitian Ini Berkembang?
Studi ini mencatat bahwa publikasi terkait LC dan AI meningkat signifikan sejak 2018, dengan puncaknya pada tahun 2022. Secara geografis, Tiongkok dan Inggris memimpin dengan masing-masing 12 dan 10 publikasi, diikuti oleh India dan Spanyol (masing-masing 4). Ini menunjukkan bahwa adopsi AI dalam konstruksi bukan hanya tren Barat, tapi juga telah menyebar luas ke Asia dan Amerika Selatan.
Scopus menjadi basis data paling dominan (63% dari total artikel), menegaskan kualitas akademik dari sumber-sumber yang dikaji.
Apa Saja Alat Lean yang Paling Populer?
Dari 24 strategi dan alat LC yang diidentifikasi, beberapa yang paling sering digunakan dalam manajemen proyek konstruksi adalah:
- Last Planner System (LPS)
Digunakan dalam 13 artikel, menjadi alat lean paling dominan. - Building Information Modeling (BIM)
Muncul dalam 25 artikel. BIM tidak hanya sebagai model visual, tapi juga integrator informasi proyek secara real-time. - Just-In-Time (JIT) dan Visual Management (VM)
Masing-masing disebut dalam lima artikel, menunjukkan popularitasnya dalam meningkatkan efisiensi lapangan.
Selain itu, alat seperti 5S, Value Stream Mapping (VSM), dan Takt Time mulai banyak digunakan dalam proyek berskala menengah.
Bagaimana AI Masuk ke Dunia Konstruksi?
AI, khususnya ML, membawa kemampuan luar biasa dalam mengolah data besar, memprediksi keterlambatan, meminimalkan risiko, dan mengoptimalkan alokasi sumber daya. Berikut adalah beberapa teknik AI yang paling banyak digunakan dalam artikel yang ditinjau:
- Artificial Neural Networks (ANN)
Teknik ML paling populer, mampu mengenali pola dan memprediksi produktivitas proyek. - Convolutional Neural Networks (CNN) dan Recurrent Neural Networks (RNN)
Digunakan dalam pengolahan visual (misalnya CCTV proyek) dan analisis waktu-berjalan. - Support Vector Machine (SVM) dan Random Forest (RF)
Banyak digunakan untuk prediksi biaya, penjadwalan, dan deteksi risiko. - Natural Language Processing (NLP)
Menjadi semakin relevan dalam membaca dokumen teknis dan kontrak otomatis.
AI tidak hanya digunakan untuk prediksi teknis, tetapi juga dalam peningkatan komunikasi antartim, pelatihan, dan pengawasan keamanan kerja secara real-time.
Studi Kritis: Apa Manfaat Kombinasi LC dan AI?
Para penulis mengelompokkan manfaat utama kombinasi LC dan AI ke dalam empat kategori besar:
1. Efisiensi Operasional
- Pengurangan pemborosan material dan waktu idle.
- Otomatisasi proses repetitive dan administratif.
- Optimasi alokasi tenaga kerja dan sumber daya.
2. Kualitas dan Keselamatan
- Monitoring lapangan secara real-time.
- Deteksi dini potensi kecelakaan.
- Laporan proyek otomatis dan akurat.
3. Optimasi Jadwal dan Anggaran
- Estimasi waktu dan biaya berbasis data historis.
- Penjadwalan dinamis berdasarkan simulasi ML.
- Peningkatan profitabilitas melalui alokasi sumber daya optimal.
4. Manajemen Risiko
- Prediksi kegagalan material atau sistem.
- Deteksi potensi delay lebih awal.
- Dukungan keputusan berbasis data probabilistik.
Studi menemukan bahwa integrasi ini tidak hanya meningkatkan performa proyek, tapi juga membentuk sistem manajemen yang lebih tangkas dan prediktif.
Apa Saja Tantangan Implementasinya?
Namun, seperti teknologi baru lainnya, integrasi LC dan AI bukan tanpa tantangan. Beberapa hambatan utama yang diidentifikasi dalam penelitian ini meliputi:
- Kualitas Data
Data proyek yang buruk atau tidak konsisten mengurangi efektivitas model ML. - Resistensi Organisasi
Banyak manajer proyek masih belum percaya dengan keputusan berbasis AI. - Kurangnya Tenaga Ahli
Kombinasi antara pengetahuan konstruksi dan kemampuan teknis AI masih langka. - Keterbatasan Infrastruktur Digital
Terutama pada proyek skala kecil-menengah atau di negara berkembang. - Masih Sedikit Studi Kasus Nyata
Mayoritas studi masih berbentuk simulasi atau proof-of-concept.
Rekomendasi: Apa Langkah Selanjutnya?
Penulis menyarankan lima arah strategis untuk mengakselerasi implementasi integrasi LC dan AI:
- Pilot Project Berskala Nyata
Lakukan uji coba di proyek konstruksi riil untuk validasi. - Pengembangan Platform Hybrid
Ciptakan tools yang menyatukan dashboard LC dan algoritma ML dalam satu sistem. - Pendidikan dan Pelatihan Terpadu
Kolaborasi antara universitas dan industri untuk menciptakan talenta lintas bidang. - Standardisasi dan Sertifikasi
Dibutuhkan standar nasional dan internasional untuk adopsi AI dalam proyek konstruksi. - Cost-Benefit Analysis Rinci
Proyek perlu menyusun model bisnis berbasis ROI dari integrasi ini.
Opini Kritis: Antara Janji dan Realisasi
Artikel ini menyajikan tinjauan yang sangat luas dan mendalam tentang lanskap integrasi LC dan AI dalam manajemen proyek konstruksi. Namun, masih ada ruang untuk eksplorasi lebih lanjut—terutama dalam pengujian solusi di proyek nyata dan pengembangan platform praktis berbasis data terbuka.
Sebagai contoh, meskipun ANN disebut-sebut sebagai algoritma paling populer, efektivitasnya bisa sangat bergantung pada jenis proyek, skala, dan ketersediaan data berkualitas. Oleh karena itu, penting untuk menghindari pendekatan “one-size-fits-all” dalam memilih teknik AI.
Penutup: Masa Depan Konstruksi Ada di Persimpangan Lean dan AI
Integrasi antara Lean Construction dan Artificial Intelligence bukan sekadar kombinasi dua buzzword. Ini adalah transformasi sistemik menuju cara kerja yang lebih cerdas, efisien, dan kolaboratif. Seiring perkembangan teknologi dan kesiapan industri, kombinasi ini bisa menjadi fondasi dari industri konstruksi 5.0—di mana efisiensi operasional, keberlanjutan, dan prediktabilitas proyek menjadi standar baru.
Bagi pemangku kepentingan di industri konstruksi—mulai dari pengembang, konsultan, hingga akademisi—saatnya tidak hanya memahami teori ini, tetapi juga berinvestasi dalam implementasi nyatanya.
Sumber asli:
Velezmoro-Abanto, L., Cuba-Lagos, R., Taico-Valverde, B., Iparraguirre-Villanueva, O., & Cabanillas-Carbonell, M. (2024). Lean Construction Strategies Supported by Artificial Intelligence Techniques for Construction Project Management—A Review. International Journal of Online and Biomedical Engineering (iJOE), 20(3), 99–114.
Building Information Modeling
BIM di Indonesia: Jalan Terjal Menuju Transformasi Digital Konstruksi
Dipublikasikan oleh Izura Ramadhani Fauziyah pada 23 April 2025
Building Information Modeling (BIM) semakin diakui sebagai game-changer dalam industri konstruksi global. Teknologi ini tidak hanya menyediakan model 3D yang informatif, tapi juga mengintegrasikan berbagai fase proyek, dari perencanaan hingga operasi dan pemeliharaan. BIM menjanjikan efisiensi biaya, pengurangan pekerjaan ulang, dan peningkatan kolaborasi antarpihak.
Namun, di Indonesia, meski implementasi BIM mulai digalakkan—termasuk pada proyek strategis nasional seperti pembangunan Ibu Kota Nusantara (IKN)—nyatanya proses adopsinya masih jauh dari ideal. Penelitian oleh Latupeirissa dkk. mengupas secara mendalam tantangan-tantangan nyata yang dihadapi dalam mengimplementasikan BIM pada proyek konstruksi nasional.
Studi Kasus Nasional: Apa Kata Praktisi Proyek?
Penelitian ini melibatkan 45 responden dari beragam latar belakang—pemilik proyek, konsultan, kontraktor swasta dan BUMN—dengan pengalaman kerja dominan di atas lima tahun. Mereka tersebar di berbagai wilayah Indonesia dan telah terlibat dalam proyek konstruksi yang mencoba menerapkan BIM, meskipun belum semua berhasil sepenuhnya.
Melalui pendekatan survei kuantitatif dan analisis korelasi linear, penelitian ini mengidentifikasi tujuh tantangan utama yang menjadi penghambat implementasi BIM secara efektif.
Tujuh Tantangan Besar Implementasi BIM di Indonesia
- Kesiapan Teknis BIM
- Tantangan ini dianggap sangat penting oleh 88,89% responden.
- BIM menuntut perangkat keras canggih, koneksi internet stabil, dan perangkat lunak berlisensi mahal. Banyak perusahaan, terutama skala menengah dan kecil, belum siap secara infrastruktur.
- Hasil analisis menunjukkan korelasi kuat antara kesiapan teknis dan keberhasilan implementasi BIM, dengan nilai r = 0,8140.
- Perubahan Paradigma Organisasi
- Sebanyak 91,11% responden mengakui adanya resistensi budaya organisasi terhadap sistem kolaboratif seperti BIM.
- Banyak manajer proyek masih nyaman dengan metode tradisional dan tidak mendorong timnya untuk berubah.
- Korelasi antara faktor ini dan adopsi BIM terbilang signifikan (r = 0,5260).
- Kesadaran Lingkungan Kerja terhadap BIM
- Meski lebih dari 93% responden menyatakan sadar akan pentingnya BIM, banyak tim proyek belum mengintegrasikan pengetahuan ini ke dalam rutinitas kerja.
- BIM sering kali dianggap sebagai tanggung jawab tim desain saja, padahal seharusnya menyentuh semua pihak.
- Nilai korelasi yang diperoleh r = 0,4730, menunjukkan hubungan moderat namun penting.
- Kepatuhan Terhadap Regulasi Terkait BIM
- Sebanyak 95,56% responden menyoroti kurangnya pemahaman dan penegakan aturan pemerintah terkait standar BIM.
- Pemerintah sebenarnya sudah mendorong penggunaan BIM pada gedung negara berukuran >2.000 m², namun pelaksanaannya belum merata.
- Korelasi r = 0,5190 mencerminkan bahwa regulasi yang belum jelas adalah penghambat yang nyata.
- Kompetensi dan Keterampilan SDM
- 95,56% menyatakan bahwa kurangnya pelatihan dan pembinaan teknis adalah hambatan besar.
- Banyak tenaga kerja konstruksi belum terpapar teknologi digital modern, apalagi BIM yang kompleks.
- Nilai korelasi r = 0,7420 menunjukkan bahwa peningkatan kapasitas SDM akan sangat menentukan keberhasilan BIM.
- Kepemimpinan yang Konsisten dan Efektif
- 97,78% responden menyadari pentingnya pemimpin proyek yang mendukung dan konsisten dalam mendorong transformasi digital.
- Sayangnya, banyak pimpinan proyek masih bertindak otoriter dan tidak membuka ruang kolaborasi.
- Nilai korelasi yang tinggi (r = 0,8550) menegaskan pentingnya kepemimpinan dalam ekosistem BIM.
- Kematangan Penggunaan BIM
- Seluruh responden (100%) sepakat bahwa belum ada standardisasi atau indikator yang jelas untuk mengukur seberapa “matang” penggunaan BIM dalam proyek mereka.
- BIM sering kali digunakan hanya untuk visualisasi 3D awal, bukan sebagai alat manajemen proyek komprehensif.
- Nilai korelasi r = 0,7630 mengindikasikan bahwa semakin matang penggunaan BIM, semakin besar peluang keberhasilan proyek secara menyeluruh.
Studi Kualitatif Tambahan: BIM dalam Proyek-Proyek Nasional
Penelitian ini menyoroti implementasi BIM pada beberapa proyek pemerintah yang patut dicermati:
- Renovasi Stadion GBK dan Manahan Solo BIM digunakan untuk mengoordinasikan desain struktural dan MEP (mekanikal, elektrikal, plumbing), serta simulasi waktu pelaksanaan.
- Pembangunan Pasar Atas Bukittinggi dan Arena PON Papua Digunakan untuk clash detection dan optimasi pemanfaatan material bangunan.
- Proyek IKN Kementerian PUPR menggandeng vendor BIM dari Singapura untuk memastikan pembangunan kota baru berjalan sesuai masterplan digital.
Namun sayangnya, keberhasilan proyek-proyek ini tidak sepenuhnya merefleksikan kondisi nasional. Implementasi BIM di sektor swasta dan proyek kecil-menengah masih jauh tertinggal, terutama karena hambatan budaya, biaya, dan SDM.
Rekomendasi Strategis untuk Mendorong Implementasi BIM
Dari hasil analisis dan wawancara, beberapa langkah strategis dapat disimpulkan:
- Pengembangan Standar Nasional
- Pemerintah perlu mempercepat penyusunan SNI atau regulasi resmi terkait BIM yang berlaku nasional.
- Sertifikasi kompetensi dan akreditasi vendor BIM perlu diatur secara ketat.
- Kampanye Kesadaran dan Pelatihan
- Sosialisasi manfaat BIM melalui seminar, workshop, dan pelatihan bersertifikat.
- Libatkan universitas dan politeknik untuk memasukkan BIM dalam kurikulum teknik sipil dan arsitektur.
- Subsidi atau Insentif Teknologi
- Pemerintah bisa memberikan potongan pajak atau subsidi software BIM untuk kontraktor lokal.
- Kemitraan dengan penyedia teknologi juga perlu didorong untuk skema sewa atau cloud-based software yang lebih murah.
- Penguatan Kepemimpinan Proyek
- Latih project manager untuk memiliki mindset digital leadership.
- Tinjau ulang struktur organisasi agar lebih horizontal dan kolaboratif.
Penutup: BIM Bukan Lagi Pilihan, Tapi Keniscayaan
Transformasi digital dalam industri konstruksi bukan sekadar tren global, tetapi kebutuhan yang mendesak. Indonesia punya potensi besar memanfaatkan BIM, namun jalan menuju ke sana masih penuh tantangan.
Penelitian ini menyajikan gambaran komprehensif dan realistis tentang kondisi implementasi BIM di Indonesia. Jika ketujuh tantangan utama yang diidentifikasi dapat diatasi secara bertahap dan terstruktur, bukan tidak mungkin BIM akan menjadi standar baru dalam setiap proyek konstruksi nasional.
Dan lebih dari itu, Indonesia bisa tampil sebagai pelopor transformasi digital di sektor konstruksi kawasan Asia Tenggara.
Sumber asli:
Latupeirissa, J. E., Arrang, H., & Wong, I. L. K. (2024). Challenges of Implementing Building Information Modeling in Indonesia Construction Projects. Engineering and Technology Journal, Volume 9, Issue 04, April 2024, pp. 3863–3871.
Teknik Industri
Teknik Sistem dan Teknik Industri
Dipublikasikan oleh Anjas Mifta Huda pada 22 April 2025
Rekayasa Sistem (SE) tumpang tindih dengan banyak bidang, seperti Teknik Industri (IE), Manajemen Rekayasa, Riset Operasi, Manajemen Proyek, dan Rekayasa Desain. Faktanya, badan pengetahuan utama Teknik Industri, yang disebut Industrial and Systems Engineering Body of Knowledge (ISEBoK) (IISE 2021), menyertakan kata “sistem” dalam judulnya dan menyertakan bagian tentang desain dan rekayasa sistem, yang merujuk pada SEBoK. Artikel ini menjelaskan persamaan dan perbedaan antara SE dan IE berdasarkan standar, buku pedoman, dan badan pengetahuan masing-masing. Berdasarkan penilaian ini, artikel ini menjelaskan peran potensial yang dilakukan oleh insinyur sistem dan insinyur industri selama siklus hidup sistem.
Pendahuluan
Ketika insinyur sistem dan insinyur industri berada dalam organisasi yang sama, mereka memiliki peran dan tanggung jawab yang berbeda. Meskipun jabatan pekerjaan berbeda-beda di setiap organisasi, banyak organisasi yang memiliki individu yang melakukan aktivitas SE dan IE. Artikel ini mencoba untuk membantu insinyur sistem dan insinyur industri untuk lebih memahami perspektif yang berbeda dari bidang tersebut dan pengetahuan yang dibutuhkan untuk memenuhi kebutuhan organisasi dan pelanggan mereka. Artikel ini membandingkan penggunaan standar internasional dan isi dari badan pengetahuan untuk SE dan IE.
Rekayasa sistem
International Council on Systems Engineering (INCOSE) adalah “organisasi keanggotaan nirlaba yang didirikan untuk mengembangkan dan menyebarluaskan prinsip-prinsip dan praktik-praktik interdisipliner yang memungkinkan terwujudnya sistem yang sukses.” INCOSE mendefinisikan rekayasa sistem sebagai
pendekatan transdisipliner dan integratif untuk memungkinkan realisasi, penggunaan, dan penghentian sistem rekayasa yang berhasil, dengan menggunakan prinsip dan konsep sistem, serta metode ilmiah, teknologi, dan manajemen. (INCOSE 2021)
Di sini, istilah “rekayasa” dan “rekayasa” digunakan dalam arti yang paling luas: “tindakan bekerja dengan penuh seni untuk menghasilkan sesuatu.” “Sistem rekayasa” dapat terdiri dari salah satu atau semua orang, produk, layanan, informasi, proses, dan elemen alam.
INCOSE menyelaraskan Buku Panduan SE-nya dengan ISO/IEC/IEEE 15288, Proses Siklus Hidup Sistem, yang berfokus pada proses. SEBoK Bagian 3 Rekayasa dan Manajemen Sistem, yang membahas proses teknis dan manajemen SE utama, juga diatur di sekitar area proses 15288. Dalam pandangan ini, SE berorientasi pada proses. Setiap edisi Buku Panduan SE selaras dengan edisi ISO/IEC/IEEE 15288. Gambar 1 menunjukkan proses 15288 dan bagaimana proses tersebut selaras dengan area topik SE Handbook dan SEBoK. Kemudian dalam artikel ini, topik dan area pengetahuan SEBoK ini dibandingkan dengan area pengetahuan IE. Area pengetahuan pada Gambar 1 selaras dengan siklus hidup sistem jika dimulai dari bagian atas kolom pertama dan dilintasi ke bawah, dilanjutkan di bagian bawah kolom kedua dan dilintasi ke atas, dan kemudian dilanjutkan di bagian bawah kolom ketiga dan dilintasi ke atas.

Sumber: sebokwiki.org Gambar 1. Topik Teknis Area Pengetahuan SEBoK yang Dipetakan ke Proses Teknis ISO/IEC/IEEE 15288. (SEBoK 2022)
Teknik industri
Institute of Industrial and Systems Engineers (IISE) menyatakan bahwa mereka adalah “satu-satunya masyarakat profesional internasional, nirlaba, yang didedikasikan untuk memajukan keunggulan teknis dan manajerial para insinyur industri.” (IISE 2021). IISE dimulai pada tahun 1948 sebagai Institut Insinyur Industri Amerika. Pada tahun 1981, organisasi ini berganti nama menjadi Institute of Industrial Engineers untuk mencerminkan keanggotaan internasionalnya yang terus berkembang. Pada tahun 2016, para anggota memilih untuk mengubah nama menjadi Institute of Industrial and Systems Engineers. Penambahan ini mencerminkan suara dari para anggotanya dan selaras dengan “perubahan ruang lingkup profesi yang, dengan tetap mempertahankan basis industrinya, telah melihat lebih banyak insinyur industri dan sistem yang bekerja dengan sistem terintegrasi berskala besar di berbagai sektor”.
Pada pergantian abad ini, teknik industri tercermin dengan baik dalam dua publikasi terkemuka: Buku Pegangan Teknik Industri (Salvendy 2001) dan edisi kelima Buku Pegangan Teknik Industri Maynard (Zandin 2001). Salvendy (2001) menyatakan bahwa insinyur industri dilatih untuk merancang dan menganalisis komponen-komponen yang menyusun sistem manusia-mesin. Mereka menyatukan elemen-elemen individual yang dirancang melalui disiplin ilmu teknik lainnya dan mensinergikan subsistem-subsistem ini secara tepat bersama dengan komponen-komponen manusia untuk sebuah sistem manusia-mesin yang terintegrasi secara menyeluruh. Insinyur industri berfokus pada peningkatan sistem apa pun yang sedang dirancang atau dievaluasi. Mereka membuat tugas manusia menjadi lebih produktif dan efisien dengan mengoptimalkan aliran, menghilangkan gerakan yang tidak perlu, memanfaatkan bahan alternatif untuk meningkatkan manufaktur, meningkatkan aliran produk melalui proses, dan mengoptimalkan konfigurasi ruang kerja. Pada dasarnya, insinyur industri bertugas untuk mengurangi biaya dan meningkatkan profitabilitas dengan memastikan penggunaan sumber daya manusia, material, fisik, dan/atau keuangan secara efisien.
Pandangan IE telah berkembang selama dua dekade terakhir. IISE mengembangkan IISE Body of Knowledge pada tahun 2021 (IISE 2021). Edisi keenam dari Buku Pegangan Teknik Industri Maynard (Zandin 2022) diharapkan akan diterbitkan pada tahun 2022. IISEBoK memiliki 14 bidang pengetahuan, seperti yang ditunjukkan pada Gambar 2. 13 area pengetahuan pertama mengidentifikasi pengetahuan Teknik Industri. Bidang keempat belas adalah Desain dan Rekayasa Sistem, yang mengacu pada SEBoK. IISEBoK memberikan penjelasan singkat tentang setiap area pengetahuan, garis besar topik area pengetahuan, dan daftar referensi. IISEBoK tidak menggunakan standar sebagai dasarnya. Faktanya, Standard Practice for Systems Safety (MIL-STD-0-882D) adalah satu-satunya standar yang dikutip di bagian referensi. IISE saat ini tidak memiliki buku panduan yang dikembangkan oleh atau untuk Institut, meskipun Zandin (2022) diharapkan dapat menyelaraskan dengan IISEBoK.

Sumber: sebokwiki.org Gambar 2. Area Pengetahuan Rekayasa Industri dan Sistem (IISE 2022, Digunakan dengan Izin) [1]
14 area topik yang termasuk dalam IISEBoK dapat dikaitkan dengan banyak standar internasional meskipun IISEBoK tidak menggunakan standar sebagai fondasinya atau memberikan referensi ke standar di sebagian besar area topiknya.
Perbandingan diagram venn
Bagian ini membandingkan kedua badan pengetahuan tersebut. Gambar 3 adalah Diagram Venn yang mengidentifikasi area pengetahuan yang biasanya dilakukan oleh insinyur sistem, yang biasanya dilakukan oleh insinyur industri, dan yang digunakan oleh kedua disiplin ilmu.

Sumber: sebokwiki.org Gambar 3. Diagram Venn (SEBoK Original
Terdapat 11 area pengetahuan utama SE, 7 area pengetahuan utama IE, dan 12 area pengetahuan yang tumpang tindih. Tabel 1 memberikan beberapa contoh ilustrasi tentang perbedaan fokus SE dan IE dalam area pengetahuan yang tumpang tindih.


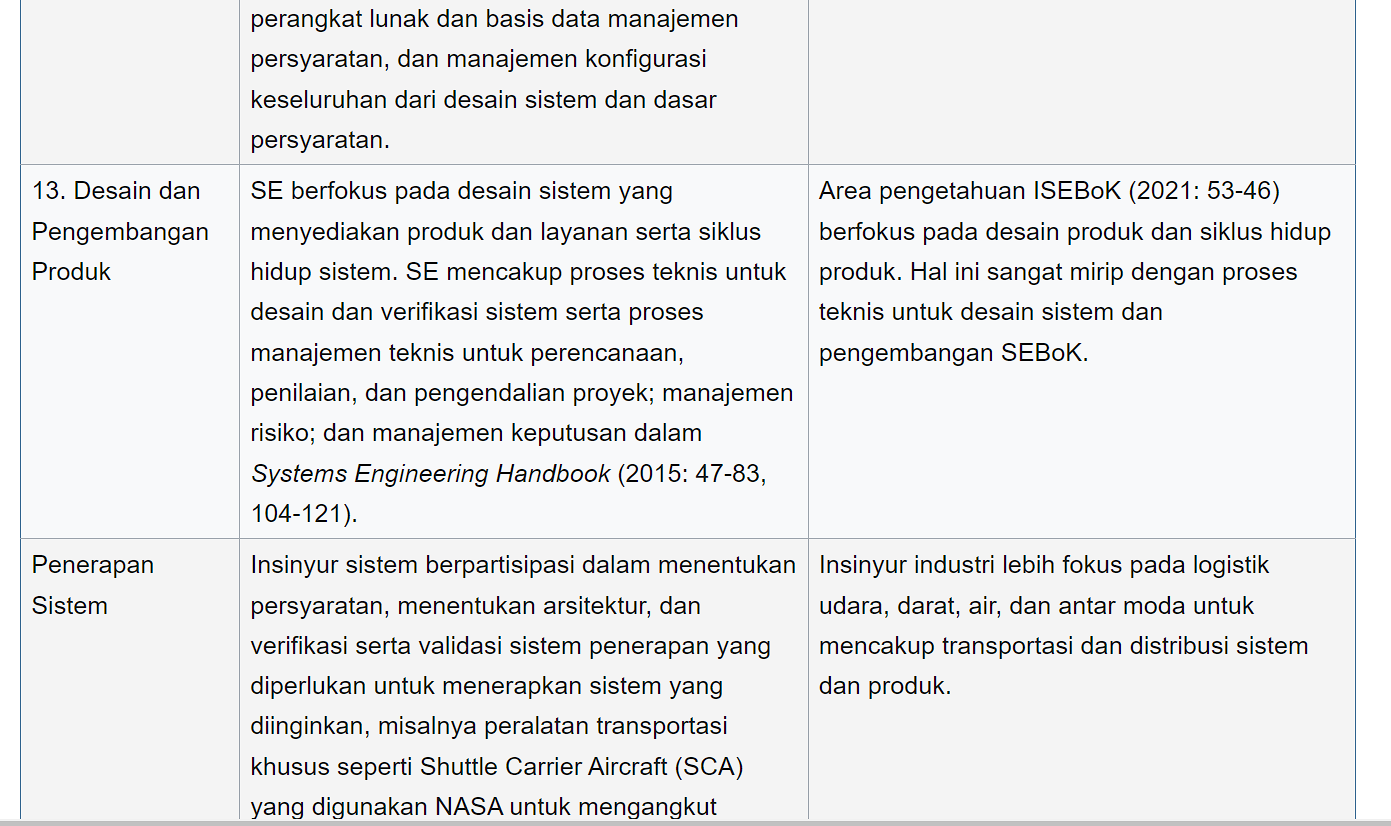
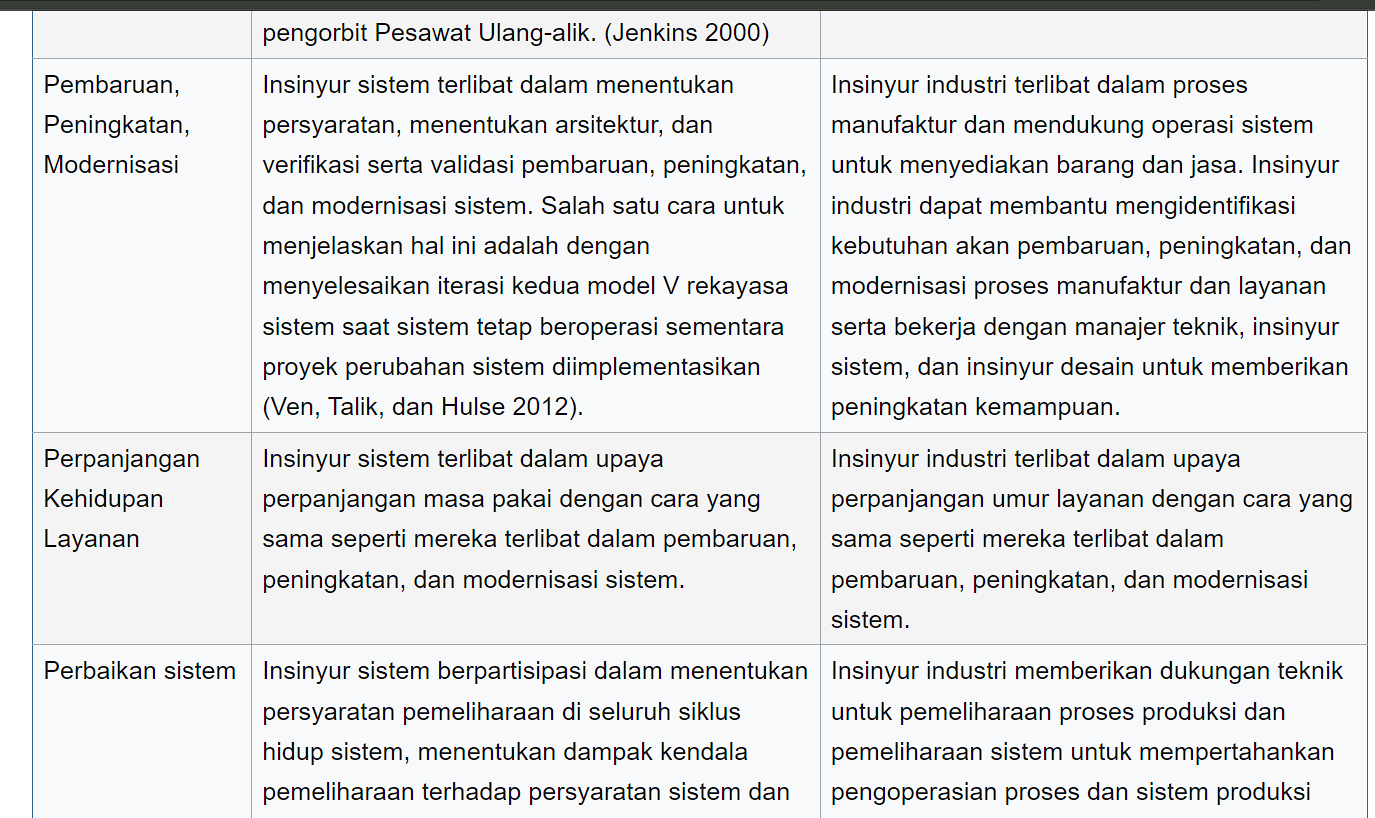
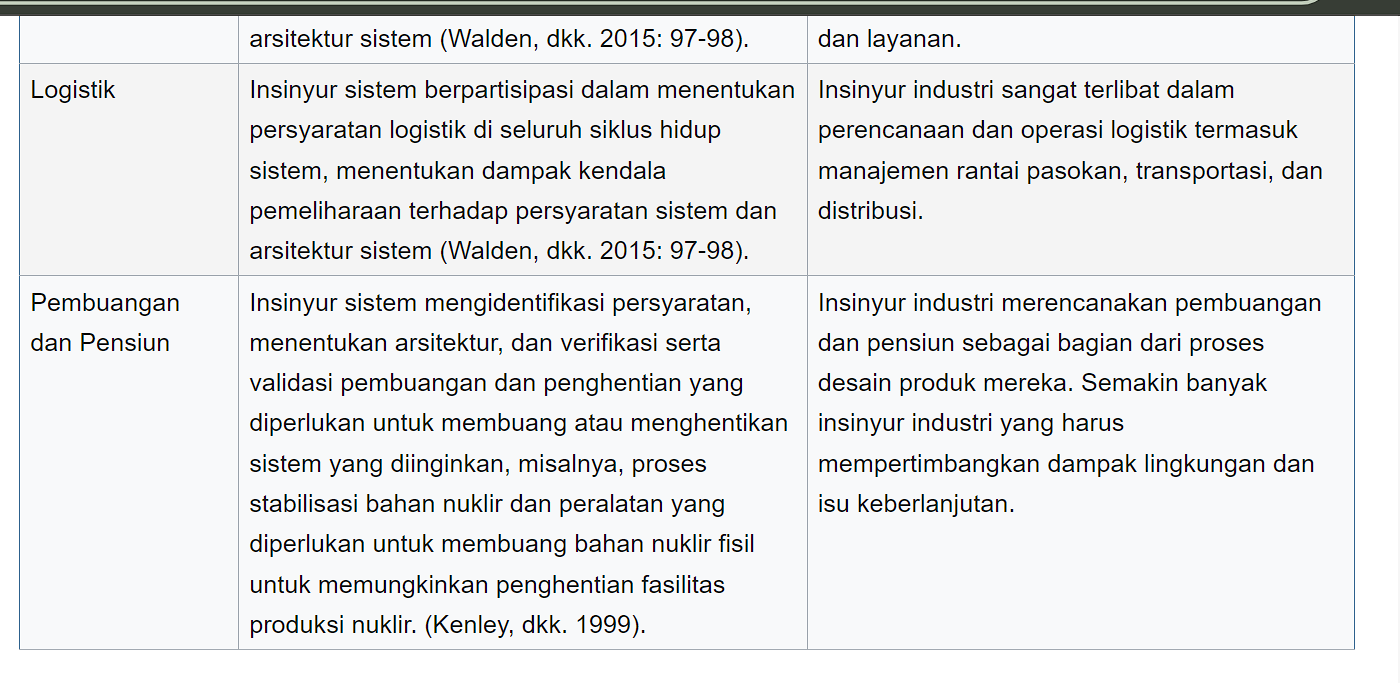
Sumber: sebokwiki.org
Peran dalam Siklus Hidup Sistem
Insinyur sistem dan insinyur industri memainkan peran penting dalam siklus hidup sistem. Gambar 4 memodifikasi format dari Buede dan Miller (2016). Gambar tersebut menunjukkan tahapan siklus hidup sistem dan, berdasarkan analisis pada bagian sebelumnya, mengidentifikasi dan merangkum peran utama insinyur sistem, insinyur industri, dan insinyur desain. Beberapa proses telah digabungkan untuk menyederhanakan gambar.

Sumber: sebokwiki.org
Disadur dari: sebokwiki.org
Teknik Industri
Identifikasi Bahaya dan Penilaian Risiko (HIRA)
Dipublikasikan oleh Anjas Mifta Huda pada 22 April 2025
Apa itu HIRA?
Studi identifikasi bahaya dan penilaian risiko (HIRA) menawarkan pendekatan sistematis untuk menilai bahaya dan risiko terkait. HIRA Safety membantu menentukan tujuan dari bahaya yang teridentifikasi dan memberikan teknik untuk mengelola risiko.
Apa yang dimaksud dengan risiko HIRA?
Ini adalah proses komprehensif penilaian bahaya, pemeriksaan risiko, dan estimasi risiko. HIRA digunakan untuk mengidentifikasi potensi bahaya dalam suatu proses atau sistem yang dapat menyebabkan kecelakaan besar, cedera, atau kerusakan lingkungan.
Setelah bahaya diidentifikasi, tim HIRA akan menilai tingkat keparahan dan kemungkinan bahaya tersebut.
Tingkat keparahan suatu bahaya adalah ukuran dari konsekuensi potensial dari bahaya, seperti jumlah orang yang dapat terluka atau intensitas kerusakan yang dapat ditimbulkan. Kemungkinan bahaya adalah ukuran seberapa besar kemungkinan bahaya tersebut terjadi.
Tim HIRA mengembangkan rekomendasi untuk menghilangkan risiko. Hal ini dapat mencakup:
- Menghilangkan bahaya sama sekali,
- Mengurangi kemungkinan terjadinya bahaya, atau
- Mengurangi tingkat keparahan konsekuensi dari bahaya.
Risiko HIRA dapat diklasifikasikan ke dalam beberapa kategori, seperti:
- Risiko proses: Ini adalah risiko yang terkait dengan proses itu sendiri, seperti risiko kebakaran atau ledakan.
- Risiko peralatan: Ini adalah risiko yang terkait dengan peralatan yang digunakan dalam proses, seperti risiko kegagalan peralatan.
- Risiko faktor manusia: Ini adalah risiko yang terkait dengan kesalahan manusia, seperti risiko pekerja melakukan kesalahan.
Mengapa HIRA penting?
Dengan mengidentifikasi dan menilai risiko, HIRA dapat membantu mengurangi kemungkinan dan tingkat keparahan Kecelakaan, Cedera, dan Kerusakan Lingkungan yang besar. Ini membantu kita:
- Untuk menentukan semua faktor yang mungkin dapat membahayakan pekerja.
- Untuk menentukan probabilitas insiden dan menganalisis tingkat keparahannya
- Mengidentifikasi perlindungan dan kontrol yang ada.
- Menilai risiko Keselamatan dan memastikan bahwa risiko tersebut masih dalam batas yang dapat diterima.
- Saran untuk mengatasi kemungkinan bahaya
HIRA dan HAZOP
HIRA dan HAZOP adalah teknik identifikasi bahaya yang digunakan dalam keselamatan Proses.
HIRA (Identifikasi Bahaya dan Penilaian Risiko) adalah metode terstruktur untuk mendeteksi dan mengevaluasi bahaya dalam fasilitas/sistem proses. HIRA mendeteksi potensi risiko yang dapat menyebabkan kecelakaan, cedera, atau kerusakan lingkungan. HIRA merupakan teknik sederhana dan mudah yang dapat digunakan untuk mengidentifikasi bahaya dalam berbagai operasi.
HAZOP (Hazard and Operational Study) adalah pendekatan yang lebih luas dan ketat untuk identifikasi dan penilaian bahaya. Tim HAZOP menggunakan seperangkat pedoman untuk mendeteksi potensi penyimpangan dari desain atau operasi yang direncanakan. Tim ini kemudian menganalisis tingkat keparahan dan kemungkinan setiap penyimpangan dan menyarankan solusi mitigasi. HAZOP merupakan prosedur yang lebih rumit dan memakan waktu dibandingkan HIRA, namun juga lebih menyeluruh dan efektif.
Data studi HIRA dan HAZOP dapat digunakan untuk membuat rencana manajemen risiko yang komprehensif. Rencana manajemen risiko harus mengidentifikasi Bahaya, menganalisis risiko, dan membuat rekomendasi mitigasi.
Organisasi dapat meningkatkan keamanan fasilitas proses mereka dan mengurangi risiko kecelakaan besar, cedera, dan kerusakan lingkungan dengan menggabungkan HIRA dengan HAZOP.
Ada berapa jenis HIRA?
Berikut ini adalah jenis-jenis penilaian risiko, Ada tiga jenis penilaian risiko yaitu Penilaian Risiko Dasar, Penilaian Risiko Berbasis Masalah, dan Penilaian Risiko Berkelanjutan.
Penilaian risiko dasar (baseline risk assessments):
Penilaian risiko baseline dilakukan untuk mengidentifikasi risiko yang terjadi pada saat pertama kali, Berdasarkan output dari penilaian risiko Baseline, aspek atau masalah yang pasti akan ditekankan. Penilaian risiko Baseline harus ditinjau pada intermisi yang direncanakan untuk memulihkan profil baseline sehingga dapat mengurangi risiko Keselamatan HIRA dalam suatu organisasi.
Penilaian risiko berbasis masalah:
Penilaian risiko berbasis masalah akan dilakukan karena aspek atau masalah yang ditekankan, terjadinya proses baru, pemasangan mesin baru, atau penilaian Bahaya yang sedang berlangsung dalam suatu organisasi.
Penilaian risiko berkelanjutan:
Penilaian risiko berkelanjutan merupakan bagian dari semua inspeksi dan observasi yang dilakukan secara rutin.
Apa saja 3 fase HIRA?
Fase 1: identifikasi bahaya
Pada fase ini, semua insiden yang mungkin terjadi ditentukan dan dikatalogkan. Kunjungan lapangan dan studi tentang semua prosedur yang terkait dengan Operasi dan dokumen Input seperti Gambar dan Proses digunakan dalam identifikasi Bahaya.
Fase 2: penilaian risiko HIRA
Masukan yang dibutuhkan
HIRA sangat bergantung pada ketersediaan dan keakuratan data input, Ketika dilengkapi dengan data Input yang lengkap, keyakinan yang lebih tinggi pada validitas dan ketahanan hasil akan diperoleh. Contoh pengumpulan data akan dikhususkan untuk operasi, desain bangunan, tingkat hunian personel/penduduk.
Metodologi penilaian risiko

Sumber: ifluids.com
Penilaian Risiko HIRA digunakan untuk manajemen risiko dan peningkatan keselamatan di beberapa industri. Metode ini memberikan penilaian kuantitatif terhadap potensi risiko yang diketahui dan memberikan dasar untuk mengevaluasi keselamatan proses dengan mengacu pada kriteria penerimaan risiko yang direncanakan.
Metode studi ini merupakan kombinasi dari identifikasi, analisis dan brain storming berdasarkan bahaya yang diidentifikasi yang dibagi menjadi empat bagian utama yang berisi beberapa kategori. Kategori yang berlaku secara umum adalah;
- Bagian 1 Bahaya Eksternal dan Lingkungan;
- Bagian 2 Bahaya Fasilitas;
- Bagian 3 Bahaya Kesehatan dan
- Bagian 4 Menilai Risiko terhadap:
- Manusia
- Aset / Produksi
- Lingkungan
Tahap 3: penghapusan risiko
Bahaya yang telah diketahui akan didaftar dan diperiksa dalam matriks risiko untuk memahami pentingnya risiko, kontrol/tindakan pengamanan akan dijelaskan berdasarkan peringkat risiko dan akhirnya rekomendasi akan diberikan untuk mencegah/menghilangkan potensi bahaya. Matriks risiko yang digunakan untuk studi ini diberikan di bawah ini


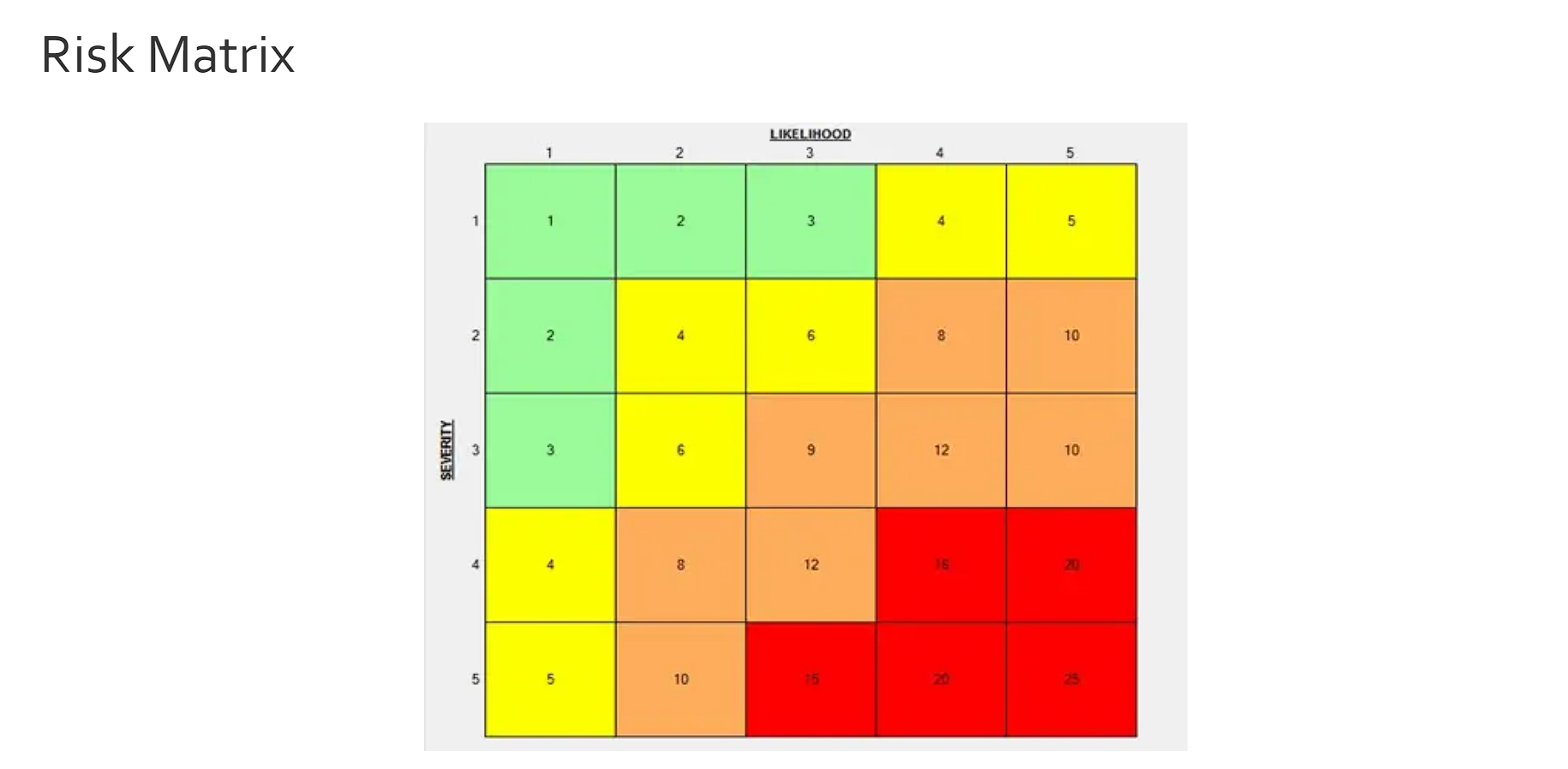

Sumber: ifluids.com
Apa saja 5 tahap penilaian risiko utama?
- Menentukan ruang lingkup penilaian risiko.
- Menentukan sumber daya yang dibutuhkan.
- Menentukan jenis tindakan analisis risiko.
- Menentukan pemangku kepentingan yang terlibat.
- Menentukan peraturan atau standar yang sesuai yang berlaku sesuai kebijakan Organisasi
Disadur dari: ifluids.co
Teknik Industri
Algoritma Evolusioner dan Metaheuristik: Aplikasi dalam Desain dan Optimasi Rekayasa
Dipublikasikan oleh Anjas Mifta Huda pada 22 April 2025
1. Pendahuluan
Algoritma evolusioner dan, secara umum, metaheuristik yang terinspirasi dari alam semakin populer sebagai metode kecerdasan komputasi, yang sangat berguna untuk masalah optimasi global. Keberhasilan kerangka kerja berbasis populasi ini terutama disebabkan oleh fleksibilitas dan kemudahan adaptasi terhadap masalah optimasi yang paling berbeda dan kompleks, tanpa memerlukan fitur atau kondisi khusus pada fungsi objektif dan kendala terkait, seperti kontinuitas, turunan, atau cembung. Masalah optimasi diskrit dan kombinatorial, serta masalah campuran, tidak menjadi batasan untuk kelas pengoptimal ini. Selain itu, persyaratan kuantifikasi ketidakpastian dalam proses pencarian, seperti dalam optimasi berbasis keandalan dan desain yang kuat, bukan merupakan batasan untuk pendekatan ini. Akhirnya, algoritma optimasi berbasis populasi dapat menangani masalah multiobjektif secara alami, dan hal ini telah membuat lompatan besar ke depan dalam kemampuan untuk menangani kelas masalah ini secara efektif. Keuntungan-keuntungan ini, bersama dengan peningkatan kinerja komputer yang stabil, mendorong peningkatan penggunaannya dalam penelitian dan industri di berbagai cabang teknik.
Metodologi ini memberdayakan peningkatan dalam desain teknik dan praktik optimasi di bidang-bidang di mana teknik optimasi klasik masih belum dapat efektif. Memang persyaratan dan batasan yang disebutkan di atas adalah hal yang biasa, seperti pemodelan yang tidak dapat dibedakan, dalam masalah rekayasa dunia nyata. Sebagai contoh, hal ini terjadi pada industri otomotif, industri penerbangan dan kedirgantaraan, serta teknik sipil, struktur, dan mesin, di mana perhitungan nilai fungsi objektif membutuhkan penyelesaian model numerik, menggunakan persamaan diferensial parsial (nonlinier), berdasarkan elemen hingga, elemen batas, volume hingga, dan sebagainya. Seperti yang dinyatakan dalam asal-usul Strategi Evolusi selama pertengahan tahun enam puluhan di Universitas Berlin (Jerman) dipicu oleh kebutuhan untuk menyelesaikan masalah “bentuk optimal benda dalam aliran” selama percobaan terowongan sayap di Institut Teknik Aliran, setelah upaya yang gagal dengan strategi koordinat dan gradien sederhana. Aplikasi awal algoritma evolusioner yang berhubungan dengan desain teknik dan optimasi dimulai pada akhir tahun delapan puluhan [3, 4] dan awal tahun sembilan puluhan seperti pada [5, 6]. Ada beberapa aplikasi yang dikompilasi dalam volume buku seperti di [7-10], dan bidang ini terus berkembang, seperti dalam kasus aplikasi multiobjektif evolusioner di mana tinjauan mutakhir dapat ditemukan di [11], atau [12, 13]. Volume terbaru dari kontribusi ilmiah di bidang ini dicakup oleh [14-16].
Kemajuan dalam penggunaan algoritma evolusioner dan metaheuristik yang terinspirasi oleh alam dalam aplikasi teknik membawa peluang dan juga tantangan bagi para peneliti untuk meningkatkan dan memajukan desain dan optimasi produk, sistem, dan layanan untuk kepentingan masyarakat. Tujuan dari edisi khusus ini adalah untuk mempublikasikan penelitian berkualitas tinggi atau artikel ulasan yang membahas perkembangan terbaru dari berbagai bidang teknik dalam kaitannya dengan penerapan algoritma evolusioner dan metaheuristik untuk desain dan optimasi, dan diharapkan dapat menstimulasi para peneliti lain untuk melanjutkan upaya untuk meningkatkan keadaan terkini dari bidang yang disebutkan di atas.
2. Kontribusi ilmiah dari edisi khusus
Dalam edisi khusus ini, proses penelaahan telah dilakukan di mana setidaknya dua penelaah per makalah telah ditugaskan, di mana tingkat penerimaan 15% telah diadakan.
Makalah yang diterima dapat diklasifikasikan menurut kategori teknik/aplikasi berikut: (a) teknik energi dan kelistrikan; (b) teknik struktur dan sipil; (c) penjadwalan transportasi dan optimasi kombinatorial; (d) kontrol; (e) aplikasi lain/militer.
Penjelasan singkat mengenai setiap kontribusi yang dipublikasikan dalam edisi khusus ini diberikan dalam paragraf-paragraf berikut ini sesuai dengan klasifikasi sebelumnya.
2.1. Teknik energi dan kelistrikan
Sebuah algoritma particle swarm optimization menggunakan strategi elang (ESPSO), sebuah metode kombinasi pencarian global dan pencarian lokal intensif, diperkenalkan untuk memecahkan masalah minimalisasi kerugian daya reaktif, oleh H. Yapıcı dan N. Cetinkaya. Eksperimen mencakup sistem daya IEEE 30-bus dan IEEE 118-bus dan subsistem distribusi daya nyata. Perbandingan dengan metaheuristik lain juga disediakan.
Rekonfigurasi smart grid dengan pembangkit terdistribusi dipelajari oleh C. Ma dkk., menggunakan optimasi particle swarm optimization hibrida ganda (algoritma optimasi particle swarm optimization biner yang lebih baik digunakan dalam pencarian grup cabang, dan algoritma pencarian optimasi particle swarm optimization biner grup yang diusulkan digunakan untuk pencarian di dalam grup). Dari simulasi pada sistem tenaga distribusi IEEE 33-bus, setelah konfigurasi ulang jaringan listrik terdistribusi, kehilangan jaringan distribusi berkurang, dan kualitas tegangan catu daya dan kualitas daya jaringan ditingkatkan.
M. Tan dkk. memperkenalkan model optimasi multiobjektif dari Masalah Penjadwalan Produksi Hot Rolling di bawah harga listrik Waktu Penggunaan, untuk meminimalkan biaya listrik secara simultan dalam produksi dan meminimalkan total penalti yang disebabkan oleh lompatan di antara lempengan yang berdekatan. Penjadwalan produksi berbasis algoritma genetika pengurutan tak berdominan (nondominated sorting genetic algorithm-II (NSGA-II)) dilakukan untuk mendapatkan solusi tak berdominan, dan metode pengambilan keputusan TOPSIS digunakan untuk pemilihan solusi akhir. Eksperimen mengkonfirmasi keberhasilan pendekatan tersebut.
2.2. teknik struktur dan sipil
J. I. Pelaez dkk. menyajikan algoritma memetika untuk desain Komposit dan Struktur Laminasi Simetris, dengan mempertimbangkan fungsi fitness kriteria ekonomi dan keamanan dalam desain dan mengimplementasikan satu set operator pencarian lokal. Algoritma ini dibandingkan dengan empat metaheuristik lainnya. Model ini telah diuji dengan desain pelat dengan pembebanan yang didistribusikan dan dibandingkan dengan dua model literatur, dan desain optimum yang divalidasi dengan paket perangkat lunak ANSYS.
F. Wu dan J. Xu menyajikan metode optimasi untuk mengevaluasi porositas reservoir yang rapat dengan menggunakan model multikomponen yang dimodifikasi menjadi model matriks campuran dan algoritma anil simulasi. Metode ini divalidasi dengan satu set data dari reservoir ketat.
Algoritma hybrid reliability-based design optimization (RBDO) diusulkan oleh H. M. Gomes dan L. L. Corso, yang menggabungkan karakteristik algoritma genetika dan particle swarm optimization dan sequential quadratic programming untuk pencarian lokal. Metode hibrida ini dianalisis berdasarkan tiga contoh benchmark RBDO rangka batang struktural untuk optimasi ukuran dengan batasan tegangan, perpindahan, dan frekuensi.
2.3. penjadwalan, transportasi, dan optimasi kombinatorial
Algoritma genetika (GA) berbasis dua fase optimasi diusulkan oleh D. Morillo dkk. untuk menyelesaikan perluasan berbasis energi dari Masalah Penjadwalan Proyek dengan Keterbatasan Sumber Daya Multimode, di mana pencarian difokuskan pada Daftar Moda dan bukan pada Daftar Aktivitas. Lima varian GA dibandingkan, di mana algoritma yang diusulkan mengungguli yang lain dalam kumpulan masalah dari pustaka masalah penjadwalan proyek PSP-LIB.
Masalah alokasi lokasi berkapasitas stokastik dua tahap dalam logistik darurat dipertimbangkan oleh Y. Deng dkk., di mana jumlah dan kapasitas pusat pasokan tidak pasti dan harus ditentukan. Untuk mengatasi masalah ini, sebuah model nilai ekspektasi dua tahap dan fungsi biaya yang digeneralisasi diusulkan. Sebuah particle swarm optimizer yang ditingkatkan dengan operator awan Gaussian, strategi restart, dan strategi parameter adaptif digunakan, serta menggunakan metode titik interior sebagai pengganti metode simpleks pada tahap kedua. Metode yang diusulkan meningkatkan presisi dan tingkat konvergensi jika dibandingkan dengan model nilai ekspektasi satu tahap klasik.
T. A. S. Masutti dan L. N. de Castro menyajikan tinjauan menyeluruh terhadap metode-metode yang terinspirasi oleh lebah yang dirancang untuk menyelesaikan masalah perutean kendaraan. Taksonomi metode dijelaskan secara rinci dan tinjauan tersebut diikuti dengan mempertimbangkan masalah yang diselesaikan dan modifikasi yang diperkenalkan dalam algoritme yang terinspirasi oleh lebah. Selain itu, algoritma TSPoptBees, modifikasi dari optBees asli yang sengaja difokuskan untuk memecahkan masalah salesman keliling (TSP), dibandingkan dengan metode optimasi lain yang terinspirasi oleh perilaku lebah untuk memecahkan satu set 28 contoh TSPLIB dengan hasil yang kompetitif.
Differential Evolution dibandingkan dengan algoritme genetika untuk menyelesaikan Electric Vehicle Routing Problem, oleh J. Barco dkk. Masalahnya didasarkan pada skema untuk mengoordinasikan penjadwalan rute dan pengisian ulang kendaraan listrik baterai (BEV), dengan mempertimbangkan biaya operasi dan degradasi baterai. Model ini didasarkan pada persamaan dinamika longitudinal gerak yang memperkirakan konsumsi energi setiap BEV, di mana studi kasus, skenario layanan antar-jemput bandara, diselesaikan.
Masalah pengemasan strip yang tidak beraturan, yang ada di banyak proses produksi di pabrik, dengan panggung persegi panjang, lebar tetap, dan panjang tidak terbatas, diselesaikan dalam penelitian yang diusulkan oleh B. A. Júnior dkk., yang menggabungkan prosedur penempatan wilayah bebas tabrakan dengan Algoritme Genetika Acak-Kunci Berfaktor Paralel dengan beberapa subpopulasi, di mana tujuannya adalah meminimalkan area yang diperlukan untuk mengalokasikan permintaan. Pendekatan ini diuji dalam satu set masalah EURO Special Interest Group on Cutting and Packing (ESICUP) dan dibandingkan dengan enam algoritma optimasi lainnya.
F. Alonso-Pecina dan D. Romero mengusulkan sebuah metode dua langkah untuk menyelesaikan Masalah Optimasi Desain Kereta Api, di mana langkah pertama bertujuan untuk menghasilkan solusi awal yang layak dan langkah kedua menggunakan simulated annealing untuk meningkatkan solusi awal, diikuti dengan prosedur yang mencoba untuk mengurangi jumlah kereta api yang dibutuhkan tanpa meningkatkan biaya keseluruhan. Eksperimen-eksperimen yang dilakukan meliputi contoh-contoh yang telah dikenal untuk memperbaiki metode-metode optimasi lainnya.
I. Stojanović dkk. menyelesaikan masalah Weber optimasi nonkonveks terkendala dengan daerah layak yang dibatasi oleh busur, dengan empat teknik swarm-intelegence: koloni lebah buatan (ABC) untuk optimasi terkendala, algoritma ABC berbasis crossover, algoritma kunang-kunang untuk optimasi terkendala, dan algoritma kunang-kunang yang disempurnakan; juga algoritma heuristik yang didasarkan pada prosedur Weiszfeld yang dimodifikasi. ABC berbasis crossover mengungguli metaheuristik lainnya (dan juga algoritma heuristik) dalam hal kualitas hasil, ketahanan, dan efisiensi komputasi, dalam eksperimen yang dipublikasikan dalam penelitian ini.
2.4. Kontrol
Metode kontrol distribusi torsi yang dioptimalkan merupakan teknologi penting untuk wheel loader listrik gandar depan/belakang (FREWL) untuk meningkatkan kinerja operasi dan efisiensi energi. Pendekatan jumlah tertimbang untuk meminimalkan rata-rata dan varians beban kerja ban dan memaksimalkan efisiensi motor total pada model dinamika longitudinal FREWL diusulkan oleh Z. Yang dkk. Algoritme pengoptimalan berikut digunakan untuk menyelesaikan masalah: metode pengali Lagrangian quasi-newton, pemrograman kuadratik berurutan, algoritme genetik adaptif, dan pengoptimalan kawanan partikel dengan pembobotan acak dan seleksi alam. Hasil penelitian mengkonfirmasi keunggulan FREWL terkontrol dibandingkan FREWL yang tidak terkontrol.
Pengontrol dual fuzzy immune Proportional-Integral-Derivative (GODFIP) diusulkan oleh A. Dai dkk., dengan mempertimbangkan penghematan energi, stabilitas, akurasi, dan kecepatan. Strukturnya terdiri dari dua pengendali fuzzy, pengendali PID, algoritma kekebalan, dan algoritma optimasi genetik. Kontroler ini dirancang dan disimulasikan untuk mengontrol radiasi inframerah dan pengering biji-bijian konveksi yang diwakili oleh model autoregressive teridentifikasi dengan input eksogen (NARX), yang meningkatkan kinerja kontroler PID imun fuzzy.
2.5. Aplikasi Lain/Militer
Masalah multiobjective weapon target assignment (WTA) di bawah ketidakpastian, yang bertujuan untuk mendapatkan efisiensi intersepsi maksimum dan konsumsi intersepsi minimum, dioptimalkan oleh H. Xu dkk., dengan multiobjective quantum-behaved particle swarm optimization dengan double/single well (MOQPSO-D/S), dan dibandingkan dengan varian PSO yang lain.
Disadur dari: hindawi.com
Teknik Industri
Apa yang dimaksud dengan Manajemen Rantai Pasok?
Dipublikasikan oleh Anjas Mifta Huda pada 22 April 2025
Manajemen rantai pasok adalah penanganan seluruh aliran produksi barang atau jasa-mulai dari komponen mentah hingga pengiriman produk akhir ke konsumen. Sebuah perusahaan menciptakan jaringan pemasok yang memindahkan produk dari pemasok bahan baku ke organisasi yang berhubungan langsung dengan pengguna.
Mengapa manajemen rantai pasok penting?
Sistem manajemen rantai pasok yang efektif meminimalkan biaya, pemborosan, dan waktu dalam siklus produksi. Standar industri telah menjadi rantai pasokan tepat waktu di mana penjualan ritel secara otomatis memberi sinyal pesanan pengisian ulang kepada produsen. Pengecer kemudian dapat mengisi kembali rak-rak hampir secepat mereka menjual produk. Salah satu cara untuk meningkatkan proses ini lebih lanjut adalah dengan menganalisis data dari mitra rantai pasokan untuk melihat di mana perlu ditingkatkan lebih lanjut.
Dengan menganalisis data mitra, CIO mengidentifikasi tiga skenario di mana manajemen rantai pasokan yang efektif dapat meningkatkan nilai pada siklus rantai pasok.
Mengidentifikasi masalah potensial
Ketika pelanggan memesan lebih banyak produk daripada yang dapat dikirim oleh produsen, pembeli dapat mengeluhkan layanan yang buruk. Melalui analisis data, produsen mungkin dapat mengantisipasi kekurangan tersebut sebelum pembeli kecewa.
Mengoptimalkan harga secara dinamis
Produk musiman memiliki umur simpan yang terbatas. Pada akhir musim, pengecer biasanya membuang produk ini atau menjualnya dengan diskon besar-besaran. Maskapai penerbangan, hotel, dan lainnya yang memiliki “produk” yang mudah rusak biasanya menyesuaikan harga secara dinamis untuk memenuhi permintaan. Dengan menggunakan perangkat lunak analitik, teknik peramalan serupa dapat meningkatkan margin, bahkan untuk barang yang tidak tahan lama.
Meningkatkan alokasi inventaris “tersedia untuk dijanjikan”
Perangkat lunak analitik membantu mengalokasikan sumber daya secara dinamis dan menjadwalkan pekerjaan berdasarkan perkiraan penjualan, pesanan aktual, dan pengiriman bahan baku yang dijanjikan. Produsen dapat mengonfirmasi tanggal pengiriman produk ketika pembeli melakukan pemesanan-secara signifikan mengurangi pesanan yang salah.
Bagaimana cara kerja manajemen rantai pasok?
Sebagian besar ahli dan praktisi mengacu pada lima komponen penting dalam manajemen rantai pasok:
Perencanaan
Rencanakan dan kelola semua sumber daya yang diperlukan untuk memenuhi permintaan pelanggan akan produk atau layanan perusahaan. Ketika rantai pasokan sudah terbentuk, tentukan metrik untuk mengukur apakah rantai pasokan tersebut efisien, efektif, memberikan nilai kepada pelanggan, dan memenuhi tujuan perusahaan.
Sumber
Pilih pemasok untuk menyediakan barang dan jasa yang dibutuhkan untuk membuat produk. Kemudian, tetapkan proses untuk memantau dan mengelola hubungan dengan pemasok. Proses utama meliputi: pemesanan, penerimaan, pengelolaan inventaris, dan otorisasi pembayaran pemasok.
Manufaktur
Mengatur kegiatan yang diperlukan untuk menerima bahan baku, memproduksi produk, menguji kualitas, mengemas untuk pengiriman, dan menjadwalkan pengiriman.
Pengiriman dan logistik
Mengkoordinasikan pesanan pelanggan, menjadwalkan pengiriman, mengirim muatan, menagih pelanggan, dan menerima pembayaran.
Pengembalian
Buat jaringan atau proses untuk mengambil kembali produk yang cacat, berlebih, atau tidak diinginkan.
Fitur-fitur utama dari manajemen rantai pasok yang efektif
Rantai pasokan adalah “wajah” bisnis yang paling jelas bagi pelanggan dan konsumen. Semakin baik dan efektif manajemen rantai pasokan suatu perusahaan, semakin baik pula perusahaan tersebut melindungi reputasi bisnis dan keberlanjutan jangka panjangnya.
IDC mendefinisikan manajemen rantai pasokan dengan mengidentifikasi lima C dari manajemen rantai pasokan yang efektif di masa depan:
- Terhubung (Connected): Mengakses data tidak terstruktur dari media sosial, data terstruktur dari Internet of Things (IoT), dan kumpulan data yang lebih tradisional yang tersedia melalui perencanaan sumber daya perusahaan (ERP) tradisional dan alat integrasi bisnis-ke-bisnis (B2B).
- Kolaboratif: Meningkatkan kolaborasi dengan pemasok semakin berarti penggunaan jaringan perdagangan berbasis cloud untuk memungkinkan kolaborasi dan keterlibatan multi-perusahaan.
- Sadar dunia maya: Memperkuat sistem dan melindunginya dari gangguan dan peretasan dunia maya merupakan perhatian penting bagi rantai pasokan perusahaan.
- Diaktifkan secara kognitif: Mengumpulkan, mengoordinasikan, dan melakukan keputusan dan tindakan di seluruh rantai pasokan, platform AI berfungsi sebagai menara kontrol rantai pasokan modern, yang memungkinkan sebagian besar rantai pasokan diotomatisasi dan belajar mandiri.
- Komprehensif: Meningkatkan kemampuan analitik dengan data secara real time untuk memastikan bahwa wawasan yang komprehensif dan cepat sangat penting, karena latensi tidak dapat diterima dalam rantai pasokan masa depan.
Banyak rantai pasok yang telah memulai proses ini, dengan partisipasi dalam jaringan perdagangan berbasis cloud yang mencapai titik tertinggi sepanjang masa dan dengan upaya besar yang sedang dilakukan untuk meningkatkan kemampuan analitik.
Evolusi manajemen rantai pasokan
Sementara rantai pasokan kemarin berfokus pada ketersediaan, pergerakan, dan biaya aset fisik, rantai pasokan saat ini adalah tentang pengelolaan data, layanan, dan produk yang digabungkan ke dalam solusi. Sistem manajemen rantai pasokan modern lebih dari sekadar di mana dan kapan. Manajemen rantai pasokan memengaruhi kualitas produk dan layanan, pengiriman, biaya, pengalaman pelanggan, dan pada akhirnya, profitabilitas.
Baru-baru ini pada tahun 2017, rantai pasokan biasa mengakses data 50 kali lebih banyak daripada lima tahun sebelumnya. Namun, para ahli hanya menganalisis kurang dari seperempat dari data ini. Itu berarti nilai dari data yang penting dan sensitif terhadap waktu-seperti informasi tentang cuaca, kekurangan tenaga kerja yang tiba-tiba, kerusuhan politik, dan lonjakan permintaan-bisa hilang.
Rantai pasokan modern memanfaatkan sejumlah besar data yang dihasilkan oleh proses rantai pasokan dan yang dikurasi oleh para ahli analisis dan ilmuwan data. Para pemimpin rantai pasokan di masa depan dan sistem ERP yang mereka kelola kemungkinan besar akan berfokus pada pengoptimalan kegunaan data ini-menganalisisnya secara real time dengan latensi minimal.
Anda dapat mengembangkan proses rantai pasok Anda menjadi alur kerja yang cerdas untuk mencapai tingkat responsif dan inovasi yang baru. Tantang proses-proses yang terkotak-kotak untuk menemukan efisiensi dan memungkinkan tim Anda untuk mengeksekusi dan menghasilkan. Gunakan teknologi baru seperti AI dan blockchain untuk membuka peluang di setiap langkah rantai nilai-mulai dari perencanaan permintaan hingga orkestrasi dan pemenuhan pesanan.
Disadur dari: www.ibm.com