Teknik Elektro
Sejarah dari Digital Signal Processor
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Sejarah Digital SIgnal Processor
Pada tahun 1976, Richard Wiggins mengusulkan konsep Speak & Spell kepada Paul Breedlove, Larry Brantingham dan Gene Frantz dari pusat penelitian Texas Instruments di Dallas. Dua tahun kemudian, pada tahun 1978, mereka memproduksi Speak & Spell pertama, pusat teknologinya adalah TMS5100, pemroses sinyal digital pertama di industri. Ini juga menetapkan tonggak sejarah lainnya, menjadi chip pertama yang menggunakan pengkodean prediktif linier untuk melakukan sintesis ucapan. Chip ini dibuat menggunakan proses manufaktur PMOS 7 µm.

TRW TDC1010 multiplier-accumulator
Pada tahun 1978, American Microsystems (AMI) merilis S2811. "Perangkat pemrosesan sinyal" AMI S2811, seperti banyak DSP selanjutnya, memiliki pengganda perangkat keras yang memungkinkannya melakukan operasi akumulasi pengganda dalam satu instruksi. S2281 adalah chip sirkuit terintegrasi pertama yang dirancang khusus sebagai DSP dan diproduksi menggunakan semikonduktor oksida logam vertikal (VMOS, V-groove MOS), sebuah teknologi yang belum pernah diproduksi secara massal.
.
Ini dirancang sebagai perangkat mikroprosesor untuk Motorola 6800 dan harus diinisialisasi oleh server. S2811 tidak sukses di pasaran. Pada tahun 1979, Intel merilis 2920 sebagai "pemroses sinyal analog". Ia memiliki ADC/DAC on-chip dengan prosesor sinyal internal, tetapi tidak memiliki pengganda perangkat keras dan tidak mencapai kesuksesan di pasar.
Pada tahun 1980, DSP mandiri pertama yang lengkap - NEC µPD7720 milik Nippon Electric Corporation berdasarkan arsitektur Harvard yang dimodifikasi dan DSP1 AT&T - didemonstrasikan di International Solid-State Circuits Conference' 80. Kedua prosesor tersebut terinspirasi oleh penelitian telekomunikasi pada masyarakat jaringan telepon aktif (PSTN). µPD7720, yang diperkenalkan untuk aplikasi pita suara, adalah salah satu DSP pertama yang sukses secara komersial. Altamira DX-1 adalah DSP awal lainnya, yang menggunakan jaringan pipa integer dengan cabang dan prediksi cabang tertunda, kesuksesan terbesar.
Ini didasarkan pada arsitektur Harvard dan karenanya demikian perintah terpisah dan memori data. Ia mempunyai serangkaian instruksi khusus, dengan instruksi seperti memuat dan mengumpulkan atau mengalikan dan mengumpulkan. Hal Ini dapat beroperasi pada angka 16-bit dan membutuhkan 390 ns untuk operasi penjumlahan dan perkalian. TI saat ini merupakan pemimpin pasar dalam DSP tujuan umum.
Sekitar lima tahun kemudian, DSP generasi kedua mulai mendapatkan popularitas. Mereka memiliki 3 memori untuk menyimpan dua operan secara bersamaan dan menyertakan perangkat keras untuk mempercepat loop ketat; Mereka juga memiliki unit pengalamatan yang mampu menangani pengalamatan loop. Beberapa di antaranya beroperasi pada variabel 24-bit, dan model tipikal hanya memerlukan sekitar 21 ns untuk MAC.
Anggota generasi ini seperti AT&T DSP16A atau Motorola 56000. Inovasi utama generasi ketiga adalah munculnya unit dan instruksi khusus aplikasi di jalur data atau terkadang sebagai koprosesor. Unit-unit ini memungkinkan akselerasi perangkat keras langsung dari masalah matematika yang sangat spesifik namun kompleks, seperti transformasi Fourier atau operasi matriks. Beberapa chip, seperti Motorola MC68356, bahkan menyertakan lebih dari satu inti pemrosesan untuk bekerja secara paralel.
DSP lain dari tahun 1995 adalah TI TMS320C541 atau TMS 320C80. Generasi keempat paling baik ditandai dengan perubahan dalam set instruksi dan pengkodean/penguraian instruksi. Ekstensi SIMD ditambahkan dan arsitektur VLIW dan superscalar muncul. Seperti biasa, kecepatan jam terus meningkat; MAC 3 ns sekarang dimungkinkan.
Disadur dari: en.wikipedia.org
Teknik Elektro
Ringkasan Definisi dari Teori Informasi
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Teori informasi adalah studi matematika tentang kuantifikasi, penyimpanan dan transmisi informasi. Bidang ini awalnya didirikan oleh karya Harry Nyquist dan Ralph Hartley pada tahun 1920-an dan Claude Shannon pada tahun 1940-an: vii Bidang matematika terapan berada di persimpangan antara teori probabilitas, statistik dan ilmu komputer, mekanika statistik, teknologi informasi dan kelistrikan. rekayasa.

Entropi percobaan Bernoulli sebagai fungsi probabilitas keberhasilan, sering disebut fungsi entropi biner, Hb(p). Entropi dimaksimalkan pada 1 bit per percobaan ketika dua kemungkinan hasil memiliki kemungkinan yang sama, seperti dalam pelemparan koin yang tidak memihak.
Entropi adalah ukuran utama teori informasi. Entropi mengukur tingkat ketidakpastian yang terkait dengan nilai variabel acak atau hasil dari proses acak. Misalnya, menentukan hasil pelemparan koin secara adil (dua kemungkinan hasil yang sama) memberikan lebih sedikit informasi (entropi lebih rendah, ketidakpastian lebih sedikit) dibandingkan menentukan hasil dengan melempar sebuah dadu (enam kemungkinan hasil yang sama). Metrik penting lainnya dalam teori informasi adalah informasi timbal balik, kapasitas saluran, eksponen kesalahan, dan entropi relatif. Bidang penting dalam teori informasi adalah pengkodean sumber, teori kompleksitas algoritmik, teori informasi algoritmik, dan keamanan teori informasi.
Penerapan topik teori data inti meliputi kompresi sumber/data (misalnya untuk file ZIP) dan pengkodean saluran/deteksi dan koreksi kesalahan (misalnya untuk DSL). Pengaruhnya sangat penting bagi keberhasilan misi luar angkasa Voyager, penemuan CD, kelayakan telepon seluler, dan perkembangan Internet. Teori ini juga dapat diterapkan di bidang lain, termasuk inferensi statistik, kriptografi, neurobiologi, persepsi, linguistik, evolusi kode dan fungsi molekul (bioinformatika), termofisika, dinamika molekul, komputasi kuantum, lubang hitam, pengambilan informasi, pengumpulan informasi, plagiarisme deteksi, pengenalan pola, deteksi anomali, dan bahkan kreasi seni.
Teori informasi mempelajari transmisi, pemrosesan, alokasi dan penggunaan informasi. Secara abstrak, informasi dapat dianggap sebagai solusi terhadap ketidakpastian. Mengenai transmisi informasi melalui saluran kebisingan, konsep abstrak ini diformalkan pada tahun 1948 oleh Claude Shannon dalam A Mathematical Theory of Communication, dimana informasi dianggap sebagai sekumpulan pesan yang mungkin dan tujuannya adalah untuk mengirimkan pesan tersebut melalui saluran kebisingan. dan biarkan penerima merekonstruksi pesan meskipun ada gangguan saluran dengan kemungkinan kesalahan yang kecil. Hasil utama Shannon, teorema pengkodean saluran berisik, menunjukkan bahwa pada batas penggunaan multisaluran, kecepatan informasi yang dapat dicapai secara asimtotik sama dengan kapasitas saluran, yang jumlahnya hanya bergantung pada statistik saluran. melalui mana pesan dikirim.
Disadur dari: en.wikipedia.org
Teknik Elektro
Mengenal Perusahaan Jepang Yaitu Intelligent Systems Co., Ltd.
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Intelligent Systems Co., Ltd, adalah pengembang video game Jepang yang terkenal dengan seri video game Fire Emblem, Paper Mario, WarioWare, dan Wars yang diterbitkan oleh Nintendo. Kantor pusat perusahaan awalnya berlokasi di Pusat Penelitian Nintendo Kyoto di Higashiyama-ku, Kyoto, namun kemudian dipindahkan ke gedung dekat kantor pusat Nintendo pada bulan Oktober 2013. Mereka juga bertanggung jawab atas pembuatan berbagai perangkat keras pengembangan yang digunakan oleh pihak pertama dan ketiga. pengembang membuat game untuk sistem Nintendo, seperti IS Nitro Emulator, kit pengembangan resmi untuk Nintendo DS.
Sejarah singkat
Sistem Cerdas dimulai ketika Nintendo mempekerjakan programmer Toru Narihiro untuk mem-porting perangkat lunak sistem disk Famicom ke format kartrid ROM standar yang digunakan di luar Jepang untuk NES. Sebagai Laboratorium HAL, tim tersebut segera menjadi utilitas Nintendo, menyediakan peralatan sistem dan mempekerjakan orang untuk memprogram, memperbaiki, atau mem-porting perangkat lunak yang dikembangkan Nintendo. Sebagian besar karya asli tim terdiri dari kontribusi kecil untuk game yang lebih besar yang dikembangkan oleh Nintendo RandD1 dan Nintendo EAD.
Narihiro memprogram video game pertamanya, Famicom Wars dan Fire Emblem: Shadow Dragon dan Blade of Light, di akhir masa pakai Famicomand#039, meskipun desain game, desain grafis, dan musiknya ditangani oleh tim RandD1 Nintendo. Berkat kesuksesan Narihiro ja#039, Intelligent Systems mulai merekrut desainer grafis, pemrogram, dan musisi untuk mengembangkan perusahaan dari pengembang utilitas menjadi tim pengembangan game. Perusahaan terus mengembangkan entri baru dalam franchise Wars dan Fire Emblem.
Intelligent Systems memproduksi Paper Mario untuk Nintendo 64 pada tahun 2000, yang menjadi kesuksesan mengejutkan yang melahirkan lima sekuel. Tiga tahun kemudian, episode pertama serial WarioWare dirilis di Game Boy Advance, dan juga menjadi serial yang sukses. Nintendo tidak mempublikasikan semua game yang dikembangkan oleh Intelligent Systems. Cubivore: Survival of the Fittest (dikembangkan bersama oleh Intelligent Systems) diterbitkan oleh Atlus di Amerika Utara; Intelligent Systems juga mengembangkan berbagai game Dragon Quest terbitan Square Enix.
Disadur dari: en.wikipedia.org
Teknik Elektro
Cahaya yang Menyampaikan Pesan: Memahami Komunikasi Optik
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Komunikasi optik, juga disebut telekomunikasi optik, memanfaatkan cahaya untuk mengirimkan informasi dari jarak jauh, baik secara visual maupun melalui perangkat elektronik. Asal-usulnya sudah ada sejak ribuan tahun yang lalu, dengan adanya fotolistrik yang ditemukan pada tahun 1880, yang menandai tonggak penting dalam komunikasi optik elektrik.
Sistem komunikasi optik terdiri dari pemancar, yang mengkodekan pesan ke dalam sinyal optik, saluran untuk transmisi sinyal, dan penerima untuk memecahkan kode pesan. Penerima dapat berupa perangkat elektronik atau individu yang menginterpretasikan sinyal visual, mulai dari nyala suar sederhana hingga lampu berkode warna yang kompleks atau urutan kode Morse.
Komunikasi optik modern sangat bergantung pada teknologi canggih seperti serat optik, laser, sakelar, dan router. Sementara sistem terestrial dibatasi oleh geografi dan cuaca, komunikasi optik ruang bebas menggunakan laser untuk mengirimkan sinyal di ruang angkasa. Artikel ini memberikan gambaran umum tentang berbagai metode komunikasi optik.
Bentuk visual
Metode komunikasi optik awal, seperti sinyal asap, api suar, dan garis semaphore, telah menjadi hal yang mendasar dalam sejarah manusia untuk menyampaikan pesan jarak jauh. Berasal dari zaman Yunani kuno, semaphore telegraf hidrolik merupakan salah satu teknik visual paling awal yang digunakan untuk komunikasi. Bahkan saat ini, suar marabahaya dan lampu navigasi terus membantu pelaut dalam keadaan darurat dan memberi tanda bahaya navigasi.
Heliograf, yang menggunakan sinar matahari yang dipantulkan oleh cermin, memungkinkan transmisi kode sinyal yang telah diatur sebelumnya melalui kilatan cahaya. Demikian pula, kapal angkatan laut menggunakan lampu sinyal dan kode Morse, sementara pilot pesawat terbang mengandalkan sistem indikator kemiringan pendekatan visual (VASI) untuk pendaratan yang aman, terutama selama operasi malam hari. Kapal induk militer juga menggunakan sistem lampu berwarna untuk pendaratan di dek yang tepat. Selain itu, menara kontrol bandara menggunakan lampu Aldis untuk berkomunikasi dengan pesawat yang mengalami gangguan radio.
- Garis Semaphore
Garis semaphore, juga dikenal sebagai telegraf optik atau semaphore Napoleon, adalah sistem awal komunikasi visual yang menggunakan menara dengan lengan atau penutup jendela yang dapat digerakkan. Pesan dikodekan berdasarkan posisi elemen mekanis ini, yang kemudian dibaca ketika penutup jendela diperbaiki. Meskipun lebih cepat daripada pengendara pos tradisional, jalur semaphore akhirnya digantikan oleh telegrafi listrik karena biayanya yang lebih tinggi dan kurangnya privasi. Jalur semaphore optik operasional pertama didirikan di Prancis pada tahun 1792 oleh Claude Chappe dan saudara-saudaranya, yang mencakup jaringan luas 556 stasiun. Meskipun terdapat variasi desain yang diadopsi oleh berbagai negara, sistem semaphore pada akhirnya menjadi usang dengan munculnya telegrafi listrik pada akhir abad ke-19.
- Bendera Semaphore
Bendera semaphore adalah sistem pensinyalan visual yang digunakan untuk menyampaikan informasi jarak jauh dengan menggunakan bendera genggam atau benda lain. Bendera, tongkat, cakram, atau dayung ini dimanipulasi untuk menyandikan pesan berdasarkan posisinya. Diadopsi secara luas di dunia maritim selama abad ke-19, bendera semaphore masih digunakan untuk komunikasi darurat di laut dan dapat diadaptasi untuk penggunaan malam hari dengan tongkat bercahaya. Sistem semaphore modern menggunakan dua tiang pendek dengan bendera persegi, dengan pemberi sinyal yang memegangnya dalam berbagai posisi untuk mewakili huruf dan angka. Warna bendera bervariasi tergantung pada apakah bendera tersebut digunakan di laut atau di darat, sehingga membantu visibilitas dan kejelasan komunikasi.
- Lampu Sinyal
Lampu sinyal, seperti lampu Aldis, berfungsi sebagai perangkat pensinyalan visual untuk komunikasi optik, yang sering kali menggunakan kode Morse. Lampu ini memancarkan pulsa cahaya yang terfokus, yang diperoleh dengan membuka dan menutup rana di depan lampu. Versi genggam menggunakan cermin cekung yang dipicu untuk memfokuskan cahaya ke dalam pulsa. Umumnya ditemukan di kapal angkatan laut dan menara kontrol bandara, lampu sinyal dilengkapi dengan pemandangan optik untuk penargetan yang tepat.
- Heliograf
Heliograf, yang berasal dari bahasa Yunani yang berarti "matahari" dan "menulis", adalah perangkat yang menggunakan sinar matahari untuk mengirim sinyal kode Morse dengan memantulkan kilatan cahaya dari cermin. Digunakan secara luas pada akhir abad ke-19 dan awal abad ke-20, terutama dalam operasi militer, survei, dan perlindungan hutan, heliograf memfasilitasi komunikasi optik yang cepat dalam jarak yang sangat jauh. Helikopter ini tetap digunakan oleh tentara Inggris dan Australia hingga tahun 1960-an dan digunakan oleh tentara Pakistan hingga tahun 1975.
Bentuk Elektronik
Bentuk elektronik sekarang banyak digunakan dalam berbagai aplikasi, termasuk kabel komunikasi serat optik dan komunikasi optik ruang bebas. Serat optik adalah saluran yang paling umum untuk komunikasi optik, dengan pemancar yang biasanya menggunakan dioda pemancar cahaya (LED) atau dioda laser. Pengkodean sinyal biasanya berupa modulasi intensitas sederhana, dan penguat serat yang didoping erbium telah memperpanjang jarak sambungan secara signifikan.
Sistem komunikasi optik pertama dirancang dan dibuat oleh Optelecom, Inc, yang didirikan oleh Gordon Gould, yang juga menemukan laser. Fotolistrik, perangkat untuk mentransmisikan suara pada seberkas cahaya, ditemukan oleh Alexander Graham Bell dan asistennya Charles Sumner Tainter pada tahun 1880. Meskipun prinsip-prinsip fotolistrik memiliki aplikasi praktis beberapa dekade kemudian, ini merupakan pencapaian terbesar Bell, karena ia menyebutnya sebagai "penemuan terbesarnya, lebih besar dari telepon."
Sistem optik ruang bebas (FSO) digunakan untuk telekomunikasi 'mil terakhir' dan dapat berfungsi pada jarak beberapa kilometer dengan garis pandang yang jelas. Sistem ini juga cocok untuk komunikasi di luar angkasa, dan banyak konstelasi satelit yang direncanakan menggunakan komunikasi laser untuk hubungan antar satelit. Transmisi sinyal optik tak terarah dikenal sebagai komunikasi nirkabel optik (OWC), yang mencakup komunikasi cahaya tampak jarak menengah dan IrDA jarak pendek menggunakan LED inframerah.
Disadur dari: en.wikipedia.org
Teknik Elektro
Stochastic Process: Mengupas Proses Acak dalam Matematika
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Dalam teori probabilitas dan bidang terkait, proses stokastik (/stəˈkæstɪk/) atau acak adalah objek matematika, biasanya didefinisikan sebagai rangkaian variabel acak dalam ruang probabilitas, di mana indeks rangkaian tersebut sering kali memiliki interpretasi temporal. Proses stokastik banyak digunakan sebagai model matematika dari sistem dan fenomena yang muncul bervariasi secara acak. Contohnya adalah pertumbuhan populasi bakteri, fluktuasi arus listrik akibat kebisingan termal, atau pergerakan molekul gas. Proses stokastik dapat diterapkan di banyak bidang keilmuan seperti biologi, kimia, ekologi, ilmu saraf, fisika, pemrosesan gambar, pemrosesan sinyal, teori kendali. teori informasi, ilmu komputer dan telekomunikasi. Selain itu, perubahan pasar keuangan yang tampaknya acak telah mendorong meluasnya penggunaan proses stokastik di bidang keuangan.

Realisasi proses gerak Wiener atau Brown yang disimulasikan komputer pada permukaan bola. Proses Wiener secara luas dianggap sebagai proses stokastik yang paling banyak dipelajari dan sentral dalam teori probabilitas.
Penerapan dan studi fenomena pada gilirannya menginspirasi proses stokastik baru. Contoh proses stokastik tersebut adalah proses Wiener atau proses gerak Brown [a] yang digunakan oleh Louis Bachelier untuk mempelajari perubahan harga di Bursa Efek Paris, dan proses Poisson yang digunakan oleh A.K. Erlang memeriksa jumlah panggilan yang dilakukan selama periode waktu tertentu. Kedua proses stokastik ini dianggap paling penting dan sentral dalam teori proses stokastik dan ditemukan berulang kali dan independen sebelum dan sesudah Bachelier dan Erlang di lingkungan dan negara yang berbeda.
Istilah fungsi acak juga digunakan untuk menunjukkan suatu proses stokastik atau acak, karena proses stokastik juga dapat diartikan sebagai elemen acak dari suatu ruang fungsi. Istilah proses stokastik dan proses acak digunakan secara bergantian, seringkali tanpa status matematika tertentu untuk sekumpulan variabel acak indeks.Namun, kedua istilah ini sering digunakan ketika variabel acak diindeks dengan bilangan bulat atau interval nyata. Jika variabel acak diindeks dalam bidang Kartesius atau ruang Euclidean yang lebih tinggi, maka himpunan variabel acak biasanya disebut bidang acak. Nilai dari suatu proses stokastik tidak selalu berupa angka, namun dapat berupa vektor atau objek matematika lainnya.
Berdasarkan sifat matematikanya, proses stokastik dapat dikelompokkan menjadi beberapa kategori, antara lain random walk, martingales, proses Markov, proses Lévy, proses Gaussian, random field, proses inovasi dan proses percabangan. Studi tentang proses stokastik menggunakan pengetahuan matematika dan teknik kalkulus probabilitas, aljabar linier, teori himpunan dan topologi dan cabang analisis matematika seperti analisis nyata, teori ukuran, analisis Fourier dan analisis fungsional. Teori proses stokastik dianggap sebagai kontribusi penting bagi matematika dan terus menjadi topik penelitian aktif baik untuk alasan teoritis maupun aplikasi.
Perkenalan
Proses stokastik atau acak dapat didefinisikan sebagai sekumpulan variabel acak yang diindeks oleh beberapa himpunan matematika, artinya setiap variabel acak dari proses stokastik terkait secara unik dengan salah satu elemen himpunan tersebut. Himpunan yang digunakan untuk menyatakan variabel acak disebut himpunan indeks. Secara historis, kumpulan indeks adalah bagian dari barisan sebenarnya, seperti bilangan asli, yang memberikan interpretasi temporal pada kumpulan indeks. Setiap variabel acak dalam himpunan mengambil nilai dari ruang matematika yang sama yang disebut ruang keadaan. Ruang keadaan ini dapat berupa, misalnya, bilangan bulat, garis real, atau ruang berdimensi Euclidean {\displaystyle n}. Pertumbuhan adalah besarnya perubahan dalam proses stokastik antara dua nilai indeks, yang sering diartikan sebagai dua titik waktu. Proses stokastik dapat memiliki banyak hasil karena keacakannya, dan salah satu hasil dari proses stokastik disebut, antara lain, fungsi sampel atau eksekusi.

Suatu contoh fungsi atau realisasi tunggal yang disimulasikan komputer, antara lain, dari proses gerak Wiener atau Brown tiga dimensi untuk waktu 0 ≤ t ≤ 2. Himpunan indeks dari proses stokastik ini adalah bilangan non-negatif, sedangkan ruang keadaannya adalah ruang Euclidean tiga dimensi.
Proses stokastik dapat dikategorikan berdasarkan berbagai faktor, seperti ruang keadaan, kumpulan indeks, atau hubungan antara variabel acak. Salah satu metode klasifikasi yang umum digunakan adalah dengan mempertimbangkan kardinalitas himpunan indeks dan ruang keadaan.
Jika dilihat sebagai waktu, sebuah proses stokastik dianggap berada dalam waktu diskrit jika himpunan indeksnya terdiri dari sejumlah elemen yang terbatas atau dapat dihitung, seperti himpunan bilangan atau bilangan asli. Sebaliknya, jika kumpulan indeks mewakili interval pada garis nyata, waktu dianggap kontinu. Kedua jenis ini masing-masing dikenal sebagai proses stokastik waktu diskrit dan waktu kontinu. Proses waktu diskrit sering kali lebih disukai untuk dipelajari karena sifatnya yang lebih sederhana, sementara proses waktu kontinu memerlukan teknik matematika yang lebih canggih.
Selanjutnya, proses stokastik diklasifikasikan berdasarkan ruang keadaannya. Jika ruang keadaan terdiri dari bilangan bulat atau bilangan asli, proses tersebut disebut sebagai proses diskrit atau bernilai bilangan bulat. Sebaliknya, jika ruang keadaan adalah garis real, proses disebut bernilai real atau memiliki ruang keadaan kontinu. Selain itu, jika ruang keadaan adalah ruang Euclidean n-dimensi, prosesnya disebut sebagai proses vektor n-dimensi.
Istilah "stokastik" pada awalnya berkaitan dengan dugaan, berasal dari kata Yunani yang berarti "membidik sasaran, menebak." Penggunaan modernnya, yang menunjukkan keacakan atau peluang, berasal dari abad ke-16. Konsep proses stokastik diperkenalkan pada abad ke-18, dengan istilah "proses stokastik" pertama kali muncul dalam bahasa Inggris pada abad ke-20.
Dalam hal notasi, proses stokastik direpresentasikan dengan simbol seperti {X(t)}, {Xt}, atau hanya X, di mana t menunjukkan himpunan indeks. Namun, penting untuk dicatat bahwa X(t) secara khusus mengacu pada variabel acak pada waktu t, bukan keseluruhan proses.
Contoh
- Proses Bernoulli
Proses Bernoulli merupakan salah satu proses stokastik yang paling sederhana, ditandai dengan urutan variabel acak yang independen dan terdistribusi secara identik (iid). Setiap variabel mengambil nilai satu atau nol, dengan probabilitas masing-masing p dan 1-p. Proses ini sering diibaratkan seperti melempar koin berulang kali, di mana probabilitas kepala koin adalah p dan ekor koin adalah 1-p. Pada dasarnya, proses Bernoulli terdiri dari variabel acak Bernoulli iid, di mana setiap lemparan koin mewakili percobaan Bernoulli.
- Random Walk
Random walk mewakili proses stokastik yang biasanya didefinisikan sebagai jumlah dari variabel atau vektor acak ke-i dalam ruang Euclidean. Proses ini berevolusi dalam waktu diskrit,[84][85][86][87][88] meskipun beberapa definisi meluas ke waktu kontinu, terutama dalam model keuangan yang menggunakan proses Wiener, yang mengarah ke beberapa kebingungan dan kritik.[90] Random walk muncul dalam berbagai bentuk, yang memungkinkan ruang negara mereka menjangkau objek matematika yang berbeda seperti kisi-kisi dan kelompok. Mereka dipelajari secara ekstensif dan menemukan aplikasi di berbagai disiplin ilmu.
- Proses Wiener
Proses Wiener, juga dikenal sebagai gerakan Brown, adalah proses stokastik yang ditandai dengan kenaikan ukuran yang stasioner dan independen terdistribusi secara normal. Dinamai dari Norbert Wiener, proses ini digunakan di berbagai bidang, awalnya memodelkan pergerakan Brownian dalam cairan.
- Proses Poisson
Proses Poisson, dengan beragam bentuk dan definisinya, merepresentasikan proses penghitungan dalam istilah stokastik. Proses ini menghitung jumlah titik atau peristiwa acak dalam interval waktu tertentu. Jumlah titik-titik ini dalam waktu tertentu mengikuti distribusi Poisson, yang ditentukan oleh parameter dan interval waktu. Dengan state space yang terdiri dari bilangan asli dan kumpulan indeks yang terdiri dari bilangan non-negatif, proses Poisson juga dikenal sebagai proses penghitungan Poisson, yang menggambarkan kegunaannya sebagai mekanisme penghitungan.
Sejarah
- Teori Probabilitas Awal
Teori probabilitas dapat ditelusuri kembali ke permainan peluang kuno, yang mendapatkan perhatian formal pada abad ke-17 melalui korespondensi Pierre Fermat dan Blaise Pascal tentang perjudian. Sebelumnya, karya Gerolamo Cardano tentang permainan peluang menjadi dasar, yang berpuncak pada "Ars Conjectandi" Jakob Bernoulli pada tahun 1713, yang menginspirasi eksplorasi lebih lanjut meskipun pada awalnya ada keengganan dari komunitas matematika.
- Mekanika Statistik
Pada abad ke-19, mekanika statistik muncul, memperlakukan sistem fisik sebagai kumpulan partikel yang bergerak. Karya James Clerk Maxwell pada tahun 1859 merevolusi bidang ini dengan memperkenalkan keacakan ke dalam teori kinetik gas, yang kemudian menjadi dasar yang berpengaruh pada model gerak Brownian Albert Einstein.
- Teori Pengukuran dan Teori Probabilitas
Proposal David Hilbert pada tahun 1900 untuk perlakuan matematis terhadap fisika dan probabilitas mendorong perkembangan teori pengukuran. Matematikawan Prancis Henri Lebesgue dan Emile Borel memelopori cabang ini, dengan buku probabilitas Paul Lévy tahun 1925 yang menandai langkah penting. Sementara itu, di Uni Soviet, ahli matematika seperti Sergei Bernstein dan Aleksandr Khinchin mulai meletakkan dasar teori probabilitas, yang berpuncak pada karya penting Kolmogorov pada tahun 1933 yang menggunakan teori ukuran untuk membangun kerangka kerja aksiomatik.
- Kelahiran Teori Probabilitas Modern
Publikasi Kolmogorov menandai lahirnya teori probabilitas modern, yang memformalkan proses stokastik dalam matematika. Kontribusi selanjutnya dari Joseph Doob, William Feller, dan lainnya mengukuhkan posisinya dalam wacana matematika, meskipun ada gangguan dari Perang Dunia II.
- Proses Stokastik setelah Perang Dunia II
Pasca Perang Dunia II, minat terhadap teori probabilitas melonjak. Karya Kiyosi Ito dalam kalkulus stokastik dan kontribusi Gilbert Hunt pada proses Markov mendorong bidang ini ke depan. Buku Joseph Doob yang berpengaruh pada tahun 1953 menekankan pentingnya teori pengukuran dalam probabilitas, yang membentuk lintasan penelitian selanjutnya.
- Penemuan Proses Stokastik Spesifik
Proses stokastik spesifik seperti proses Bernoulli dan random walk memiliki sejarah panjang, dimulai dari penelitian Jakob Bernoulli pada abad ke-18. Eksplorasi Albert Einstein tentang gerak Brown pada tahun 1905 dan karya perintis Louis Bachelier dalam matematika keuangan meletakkan dasar yang penting. Proses Siméon Poisson muncul dalam berbagai konteks, terutama dalam model asuransi Filip Lundberg pada tahun 1903 dan model panggilan telepon A.K. Erlang pada tahun 1909. Kontribusi Andrey Markov pada awal abad ke-20 meletakkan dasar untuk proses Markov, dengan perkembangan selanjutnya oleh Maurice Fréchet dan lainnya yang membentuk evolusi bidang ini. Proses Lévy, yang dinamai sesuai nama Paul Lévy, mendapat kontribusi dasar dari Bruno de Finetti dan Kiyosi Itô pada tahun 1930-an.
Disadur dari: en.wikipedia.org
Teknik Elektro
Antarmuka Pengguna (UI): Mengupas Konsep dan Peran Masing-Masing
Dipublikasikan oleh Sirattul Istid'raj pada 29 April 2025
Antarmuka pengguna (dalam bahasa Inggris: user interface; disingkat UI) adalah suatu bentuk tampilan grafis yang berhubungan langsung dengan pengguna. Antarmuka pengguna berfungsi untuk menghubungkan pengguna dengan sistem operasi agar komputer dapat digunakan.

The Reactable, contoh antarmuka pengguna yang nyata
Dalam desain industri interaksi manusia-komputer, antarmuka pengguna (UI) adalah ruang tempat terjadinya interaksi antara manusia dan mesin. Tujuan dari komunikasi ini adalah untuk memungkinkan penggunaan dan pengendalian mesin secara efisien oleh manusia, sementara mesin mengembalikan informasi yang membantu pengguna dan #039; keputusan membuat proses. Contoh konsep antarmuka pengguna yang luas ini mencakup aspek interaktif sistem operasi komputer, perkakas tangan, kendali mesin berat, dan kendali proses. Pertimbangan desain yang diterapkan pada pembuatan antarmuka pengguna berkaitan dengan disiplin ilmu seperti ergonomi dan psikologi.
Secara umum, tujuan dari desain antarmuka pengguna adalah untuk menghasilkan antarmuka pengguna yang membuat penggunaan mesin menjadi mudah, efisien, dan menyenangkan (user-friendly) dengan cara yang menghasilkan hasil yang diinginkan (yaitu kegunaan maksimal). Ini biasanya berarti bahwa pengguna harus memberikan masukan sesedikit mungkin untuk mencapai keluaran yang diinginkan, dan juga mesin meminimalkan keluaran yang tidak diinginkan kepada pengguna.
Antarmuka pengguna terdiri dari satu atau lebih lapisan, termasuk antarmuka manusia-mesin (HMI), yang biasanya menghubungkan mesin ke perangkat keras masukan fisik (seperti keyboard, mouse, atau gamepad) dan perangkat keras keluaran (seperti monitor komputer, speaker, dan printer ). Perangkat yang mengimplementasikan antarmuka pengguna disebut antarmuka manusia (HID). Antarmuka yang menghilangkan pergerakan fisik bagian tubuh sebagai langkah perantara antara otak dan mesin tidak menggunakan perangkat input atau output selain elektroda; mereka disebut antarmuka otak-komputer (BCI) atau antarmuka otak-komputer (BMI).
Istilah lain untuk antarmuka manusia-mesin adalah antarmuka manusia-mesin (MMI) dan, untuk komputer, antarmuka manusia-komputer. Lapisan antarmuka pengguna tambahan dapat berinteraksi dengan satu atau lebih indera manusia, termasuk: antarmuka pengguna taktil (sentuhan), antarmuka pengguna visual (penglihatan), antarmuka pendengaran (suara), antarmuka penciuman (penciuman), antarmuka pengguna keseimbangan (keseimbangan), dan pengecapan. . antarmuka pengguna (rasa). .
Antarmuka pengguna komposit (CUI) adalah antarmuka pengguna yang berinteraksi dengan dua pikiran atau lebih. CUI yang paling umum adalah antarmuka pengguna grafis (GUI), yang terdiri dari antarmuka sentuh dan antarmuka visual yang mampu menampilkan grafik. Ketika audio ditambahkan ke antarmuka pengguna grafis, itu menjadi antarmuka pengguna multimedia (MUI). Ada tiga kategori besar CUI: standar, virtual, dan ditingkatkan. CUI standar menggunakan perangkat antarmuka manusia standar seperti keyboard, mouse, dan monitor komputer. Ketika CUI memblokir dunia nyata untuk menciptakan realitas virtual, CUI adalah virtual dan menggunakan antarmuka realitas virtual. Jika CUI tidak mencakup dunia nyata atau menciptakan augmented reality, CUI tersebut ditambah dan menggunakan antarmuka augmented reality.
Ketika antarmuka pengguna berinteraksi dengan semua indera seseorang, itu disebut antarmuka qualia, dinamai berdasarkan teori qualia. [rujukan?] CUI juga dapat diklasifikasikan berdasarkan berapa banyak indera yang berinteraksi dengannya, baik antarmuka realitas virtual sensorik X atau antarmuka pengguna realitas tertambah X., di mana X adalah jumlah indra yang terhubung. Misalnya, Smell-O-Vision adalah antarmuka standar 3-indera (3S) dengan tampilan visual, suara, dan penciuman. ketika realitas virtual menghubungkan antarmuka dengan penciuman dan sentuhan, itu dikatakan sebagai antarmuka realitas virtual 4-indera (4S); dan ketika antarmuka augmented reality mencakup penciuman dan sentuhan, itu dikatakan sebagai antarmuka augmented reality empat indera (4S).
Review
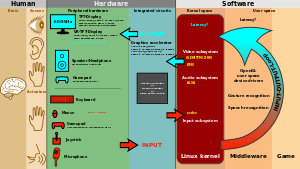
Antarmuka manusia-mesin biasanya melibatkan perangkat keras periferal untuk INPUT dan OUTPUT. Seringkali, ada komponen tambahan yang diimplementasikan dalam perangkat lunak, seperti misalnya. antarmuka pengguna grafis.
Antarmuka pengguna, atau antarmuka manusia-mesin, adalah bagian mesin yang berhubungan dengan komunikasi manusia-mesin. Sakelar membran, keyboard karet, dan layar sentuh adalah contoh bagian fisik antarmuka manusia-mesin yang dapat kita lihat dan sentuh.
Dalam sistem yang kompleks, antarmuka manusia-mesin biasanya berbasis komputer. Antarmuka manusia-komputer mengacu pada sistem seperti itu. Dalam konteks komputasi, istilah ini biasanya meluas ke perangkat lunak yang dirancang untuk mengontrol elemen fisik yang digunakan dalam interaksi manusia-komputer. Antarmuka manusia-mesin ditingkatkan dengan mempertimbangkan ergonomi (faktor manusia). Disiplin terkait adalah rekayasa faktor manusia (HFE) dan rekayasa kegunaan (UE), yang merupakan bagian dari rekayasa sistem.
Disadur dari: en.wikipedia.org