Butana, juga dikenal sebagai n-butana, adalah alkana dengan rumus kimia C4H10. Butana adalah gas yang sangat mudah terbakar dan tidak berwarna yang mudah mencair dan menguap pada suhu dan tekanan kamar. Nama "butana" berasal dari "asam butirat," yang pada gilirannya berasal dari kata Yunani untuk mentega. Ditemukan dalam minyak mentah pada tahun 1864 oleh Edmund Ralds, sifat-sifatnya pertama kali dijelaskan olehnya. Walter O. Snelling mengkomersialkan butana pada awal tahun 1910-an. Butana diklasifikasikan sebagai salah satu gas minyak bumi cair (gas LP), bersama dengan propana, propilena, dan lainnya. Butana terbakar lebih bersih daripada bensin dan batu bara.
Sejarah singkat
Sintesis awal butana terjadi secara tidak sengaja pada tahun 1849 oleh ahli kimia Inggris Edward Frankland dari etil iodida dan seng, meskipun ia salah mengidentifikasi zat yang dihasilkan. Berbagai nama digunakan untuk butana pada tahun 1860-an, termasuk "hidrida butil", "butil hidrida", "hidrida tetril", "tetril hidrida", "dietil", "etil etilida", dan lain-lain. Pada tahun 1866, Wilhelm von Hofmann mengusulkan istilah "quartana" dalam nomenklatur sistematisnya, dan nama modern diadopsi dalam bahasa Inggris dari bahasa Jerman sekitar tahun 1874.
Butana memiliki penggunaan praktis yang terbatas hingga tahun 1910-an ketika W. Snelling menyadari potensinya sebagai komponen dalam bensin. Dia menemukan bahwa ketika didinginkan, baik butana maupun propana dapat disimpan dalam kondisi cair yang dikurangi volumenya dalam wadah bertekanan.
Kepadatan Senyawa
Kepadatan butana bervariasi secara signifikan berdasarkan kondisi suhu dan tekanan di reservoir. Misalnya, pada tekanan hingga 2MPa dan suhu 27±0,2 °C, massa jenis butana cair kira-kira 571,8±1 kg/m3. Namun, pada kondisi tekanan yang sama tetapi pada suhu -13±0,2 °C, densitas butana cair meningkat menjadi sekitar 625,5±0,7 kg/m3.
Isomer
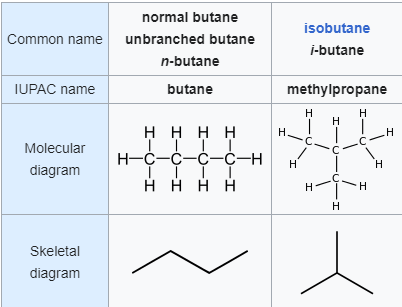
Rotasi terhadap ikatan C−C pusat menghasilkan dua konformasi berbeda (trans dan gauche) untuk n-butana
Reaksi Senyawa
Ketika butana terbakar dengan adanya oksigen yang melimpah, butana akan membentuk karbon dioksida dan uap air. Namun, jika oksigen terbatas, butana dapat menghasilkan karbon (jelaga) atau karbon monoksida. Butana lebih berat daripada udara. Dalam kondisi dengan oksigen yang cukup:
2 molekul butana (C4H10) bereaksi dengan 13 molekul oksigen (O2) menghasilkan 8 molekul karbon dioksida (CO2) dan 10 molekul air (H2O).
Dalam situasi dengan oksigen terbatas:
2 molekul butana (C4H10) bereaksi dengan 9 molekul oksigen (O2) untuk menghasilkan 8 molekul karbon monoksida (CO) dan 10 molekul air (H2O). Berdasarkan beratnya, butana mengandung sekitar 49,5 MJ/kg atau 29,7 megajoule per liter dalam bentuk cair. Suhu nyala api adiabatik maksimumnya dengan udara adalah 2.243 K.
n-Butana berfungsi sebagai bahan baku untuk proses katalitik DuPont untuk memproduksi maleic anhydride. Selain itu, seperti semua hidrokarbon, ia mengalami klorinasi radikal bebas, menghasilkan 1-kloro dan 2-klorobutana, bersama dengan turunan terklorinasi lainnya. Tingkat klorinasi yang bervariasi disebabkan oleh energi disosiasi ikatan yang berbeda dari ikatan C-H yang terlibat.
Penggunaan
Butana normal dapat digunakan untuk pencampuran bensin, sebagai bahan bakar gas, pelarut ekstraksi wewangian, baik secara terpisah maupun dalam campuran dengan propana, dan sebagai bahan baku pembuatan etilena dan butadiena, bahan utama karet sintetis. Isobutana terutama digunakan oleh kilang untuk meningkatkan (meningkatkan) angka oktan bensin motor.
Untuk pencampuran bensin, n-butana adalah komponen utama yang digunakan untuk memanipulasi tekanan uap Reid (RVP). Karena bahan bakar musim dingin membutuhkan tekanan uap yang jauh lebih tinggi agar mesin dapat dihidupkan, kilang menaikkan RVP dengan mencampurkan lebih banyak butana ke dalam bahan bakar. n-Butana memiliki angka oktan penelitian yang relatif tinggi (RON) dan angka oktan motorik (MON), yaitu masing-masing 93 dan 92.
Ketika dicampur dengan propana dan hidrokarbon lainnya, campuran tersebut dapat disebut secara komersial sebagai gas minyak cair (LPG). Butana digunakan sebagai komponen bensin, sebagai bahan baku untuk produksi petrokimia dasar dalam perengkahan uap, sebagai bahan bakar untuk pemantik rokok dan sebagai propelan dalam semprotan aerosol seperti deodoran. Bentuk murni butana, terutama isobutana, digunakan sebagai refrigeran dan sebagian besar telah menggantikan halometana perusak lapisan ozon di lemari es, freezer, dan sistem pendingin udara.
Tekanan operasi untuk butana lebih rendah daripada halometana seperti Freon-12 (R-12), sehingga sistem R-12 seperti yang ada di sistem pendingin udara otomotif, ketika diubah menjadi butana murni, akan berfungsi dengan buruk. Sebagai gantinya, campuran isobutana dan propana digunakan untuk memberikan kinerja sistem pendingin yang sebanding dengan penggunaan R-12.
Butana juga digunakan sebagai bahan bakar korek api atau obor butana dan dijual dalam kemasan sebagai bahan bakar untuk memasak, barbekyu, dan kompor berkemah. Pada abad ke-20, perusahaan Braun dari Jerman membuat produk alat penata rambut tanpa kabel yang menggunakan butana sebagai sumber panas untuk menghasilkan uap. Sebagai bahan bakar, butana sering dicampur dengan sejumlah kecil merkaptan untuk memberikan gas yang tidak terbakar dengan bau yang mudah terdeteksi oleh hidung manusia.
Dengan cara ini, kebocoran butana dapat dengan mudah diidentifikasi. Meskipun hidrogen sulfida dan merkaptan bersifat toksik, namun keduanya hadir dalam kadar yang sangat rendah sehingga bahaya mati lemas dan kebakaran oleh butana menjadi perhatian jauh sebelum toksisitas. Sebagian besar butana yang tersedia secara komersial juga mengandung minyak kontaminan, yang dapat dihilangkan dengan penyaringan dan jika tidak, akan meninggalkan endapan pada titik penyalaan dan pada akhirnya dapat menghalangi aliran gas yang seragam. Butana yang digunakan sebagai pelarut untuk ekstraksi wewangian tidak mengandung kontaminan ini dan gas butana dapat menyebabkan ledakan gas di area yang berventilasi buruk jika kebocoran tidak diketahui dan dinyalakan oleh percikan atau nyala api.
Efek dan masalah kesehatan
Menghirup butana dapat menyebabkan euforia, mengantuk, pingsan, sesak napas, aritmia jantung, fluktuasi tekanan darah, dan kehilangan ingatan sementara, jika disalahgunakan secara langsung dari wadah yang bertekanan tinggi, dan dapat menyebabkan kematian akibat sesak napas dan fibrilasi ventrikel. Butana masuk ke dalam suplai darah dan dalam hitungan detik menyebabkan keracunan.
Butana adalah zat mudah menguap yang paling sering disalahgunakan di Inggris, dan merupakan penyebab 52% kematian yang terkait dengan pelarut pada tahun 2000. Dengan menyemprotkan butana langsung ke tenggorokan, semburan cairan dapat mendingin dengan cepat hingga -20 ° C (-4 ° F) melalui ekspansi, menyebabkan kejang tenggorokan yang berkepanjangan. Sindrom "Kematian mendadak", yang pertama kali dideskripsikan oleh Bass pada tahun 1970, merupakan penyebab tunggal kematian terkait pelarut yang paling umum, yang mengakibatkan 55% kasus fatal yang diketahui.
Disadur dari: en.wikipedia.org