Teknik Kimia
Optimalisasi Formulasi Nimesulid dengan Pendekatan Quality by Design (QbD): Resensi Konseptual dan Reflektif
Dipublikasikan oleh Hansel pada 11 November 2025
Pendahuluan
Dalam era farmasi modern, tantangan terhadap kelarutan zat aktif menjadi hambatan utama dalam efektivitas terapeutik obat. Salah satu pendekatan yang menjanjikan untuk mengatasi masalah ini adalah Quality by Design (QbD), sebuah filosofi sistematik yang menekankan pentingnya desain berbasis pengetahuan dan kontrol proses dalam pengembangan produk farmasi. Tesis yang ditulis oleh Hala Khamis dari Near East University ini mengusung tema "QbD Approach Formulation Design for Poorly Soluble Drug Nimesulid and Evaluations" yang menawarkan eksplorasi mendalam terhadap strategi formulasi menggunakan model obat dengan kelarutan rendah, yakni Nimesulid.
Latar Belakang Teoritis dan Konteks Formulasi Nimesulid
Karakteristik Nimesulid dan Tantangannya
Nimesulid adalah obat antiinflamasi non-steroid (NSAID) yang digunakan secara luas, namun dibatasi oleh bioavailabilitas rendah karena kelarutannya yang buruk dalam air (0.01 mg/ml). Obat ini termasuk dalam kelas II BCS: kelarutan rendah, permeabilitas tinggi. Bentuk kristalnya terdiri dari dua polimorf: bentuk I yang stabil namun kurang larut, dan bentuk II yang metastabil namun lebih larut. Perbedaan solubilitas yang signifikan antara keduanya (4.3 kali lebih larut bentuk II) menjadi kunci dalam strategi formulasi.
Kerangka Quality by Design (QbD)
QbD menurut panduan ICH Q8 mengedepankan identifikasi atribut kritis, desain ruang operasi optimal, serta pemantauan dan kontrol terhadap parameter proses penting. Dalam studi ini, QbD digunakan tidak sekadar sebagai kerangka formal, tetapi sebagai metodologi eksploratif untuk:
- Mengidentifikasi Critical Quality Attributes (CQA) dan Critical Process Parameters (CPP).
- Menetapkan Target Product Profile (TPP) dan Quality Target Product Profile (QTPP).
- Menggunakan perangkat lunak Modde untuk eksplorasi ruang desain (design space).
Rancangan Metodologi: Kombinasi Eksipien dan Simulasi Kompaksi
Penelitian ini menggunakan metode Direct Compression (DC), didukung oleh simulasi kompaksi pada dua gaya tekan: 5 dan 10 kN. Eksipien utama meliputi:
- Filler: Flowlac®100 dan Avicel®102
- Binder: Kollidon®30
- Superdisintegrant: Kollidon®CL dan Primojel®
- Lubrikan: Magnesium stearat
Pendekatan ini memungkinkan pengujian berbagai komposisi dengan efisiensi tinggi, serta menghasilkan pemahaman lebih dalam terhadap pengaruh eksipien terhadap disintegrasi dan pelepasan obat.
Temuan Eksperimental dan Refleksi Teoretis
Analisis Kelarutan dan Karakterisasi Fisik
- Solubilitas maksimum Nimesulid di buffer pH 7.4 (dengan 0.5% Tween-80): **0.0776 mg/ml**.
- NS (produk pasar) digunakan sebagai kontrol referensi.
- Formulasi KOK5b (100 mg Nimesulid) menunjukkan kesamaan (f2 = 61.4) dengan NS, memenuhi standar penerimaan kesetaraan disolusi.
Interpretasi teoretis dari hasil ini mempertegas peran surfaktan non-ionik (Tween-80) dalam meningkatkan solubilitas obat yang bersifat lipofilik. Angka f2 menunjukkan efikasi pendekatan QbD dalam menghasilkan profil disolusi sebanding dengan produk komersial.
Pengaruh Superdisintegrant dan Binder
- Kollidon®CL menunjukkan pelepasan obat lebih tinggi dibanding Primojel® dalam formulasi tanpa binder.
- Formulasi tanpa binder menghasilkan hasil disolusi lebih baik dan kinerja fisik memadai.
- Hasil uji pada gaya tekan 10 kN menunjukkan bahwa peningkatan kadar binder justru memperlambat disintegrasi.
Hasil ini menunjukkan adanya ambiguitas dalam fungsi eksipien: binder yang diharapkan memperkuat tablet justru dapat memperlambat disolusi jika melebihi ambang optimal. Di sisi lain, superdisintegrant memiliki sensitivitas tinggi terhadap kadar dan tekanan kompaksi.
Analisis Naratif Argumentatif dan Struktur Ilmiah
Studi ini dibangun dengan struktur logis dan argumentasi berjenjang:
- Masalah dasar: Nimesulid memiliki kelarutan rendah.
- Solusi konseptual: Penerapan QbD sebagai pendekatan sistemik.
- Pendekatan praktis: Formulasi DC dan analisis CQA.
- Validasi empiris: Data disolusi dan hasil kesetaraan bio.
Penulis secara konsisten menyelaraskan kerangka teori QbD dengan eksperimen laboratorium, menegaskan bahwa kualitas dapat dirancang sejak awal melalui pemahaman interaksi material-proses.
Kritik terhadap Pendekatan Metodologis
Meskipun studi ini menyajikan eksplorasi komprehensif, terdapat beberapa kritik metodologis:
Keterbatasan desain eksperimental: Hanya dua level tekanan (5, 10 kN) diuji, padahal respon eksipien bisa non-linear pada tekanan di atas atau di bawahnya.
Fokus utama pada fisika, bukan biofarmasetika:** Tidak ada simulasi pelepasan in-vivo atau korelasi IVIVC.
Minimnya evaluasi jangka panjang: Stabilitas polimorf II tidak diuji dalam penyimpanan jangka panjang, padahal bentuk metastabil rentan bertransformasi.
Kritik ini bukan untuk menegasikan kontribusi, melainkan untuk memperkaya diskusi keilmuan dan membuka ruang eksplorasi lanjutan.
Kontribusi Ilmiah dan Implikasi
Tesis ini memberikan kontribusi nyata dalam tiga ranah:
1. Konseptual: Memperluas penerapan QbD dari sekadar regulatory compliance menjadi pendekatan eksploratif dalam desain formulasi.
2. Empiris: Menyediakan data konkret tentang efek binder dan disintegran dalam sistem Nimesulid.
3. Praktis: Menawarkan komposisi formulasi alternatif tanpa binder yang lebih efisien.
Implikasi ilmiahnya mencakup potensi penggunaan pendekatan serupa untuk obat BCS kelas II lainnya, serta dorongan terhadap pemanfaatan Modde atau perangkat DoE lainnya dalam desain obat generik.
Penutup
Dengan mengadopsi pendekatan Quality by Design secara konseptual dan praktis, studi ini berhasil menunjukkan bagaimana desain formulasi dapat dikendalikan dan dioptimalkan melalui pemahaman mendalam atas interaksi antar-eksipien dan parameter proses. Temuan bahwa formulasi tanpa binder dapat memberikan performa disolusi superior membuka kemungkinan baru dalam desain tablet untuk zat aktif yang sulit larut. Ini bukan hanya menjadi solusi teknis, tapi juga langkah epistemologis menuju farmasetika yang lebih prediktif, efisien, dan berbasis ilmiah.
Teknik Kimia
Optimalisasi Proses Berbasis Quality by Design (QbD) dalam Pengembangan Partikel Fungsional dengan Teknik Pelapisan Kering: Pendekatan Konseptual dan Reflektif
Dipublikasikan oleh Muhammad Reynaldo Saputra pada 02 Agustus 2025
Pendahuluan: Transformasi Paradigma Mutu di Industri Farmasi
Dalam lanskap industri farmasi yang terus berkembang, pendekatan tradisional Quality by Testing (QbT) mulai kehilangan relevansi akibat ketergantungannya pada kontrol kualitas pasca-produksi yang mahal dan tidak efisien. Artikel ini menggagas pendekatan alternatif yang lebih proaktif, yakni Quality by Design (QbD), yang tidak hanya menjamin kualitas, tetapi menanamkannya sejak tahap desain produk.
Penelitian oleh Dahmash et al. memperlihatkan aplikasi sistematis prinsip QbD dalam mengoptimalkan proses pelapisan partikel kering (dry particle coating) guna menghasilkan partikel fungsional (functionalised particles/FP) dengan karakteristik pelepasan terkontrol. Penelitian ini menyuguhkan kerangka konseptual yang kuat, menyandingkan risiko, eksperimen terkontrol, dan validasi statistik dalam satu narasi logis.
Kerangka Teori: Integrasi QbD dalam Teknik Pelapisan Kering
QbD merupakan pendekatan berbasis risiko yang mengharuskan identifikasi dan kontrol atas Critical Process Parameters (CPPs) yang memengaruhi Critical Quality Attributes (CQAs). Penelitian ini menyelaraskan seluruh tahapan QbD—mulai dari penetapan Quality Target Product Profile (QTPP), penilaian risiko, hingga perancangan eksperimen (Design of Experiments/DOE)—dengan proses pelapisan kering untuk meningkatkan efektivitas sistem pengembangan farmasi.
Teknik pelapisan kering sendiri mengandalkan adhesi partikel tamu (ibuprofen) ke partikel pembawa (MCC) melalui gaya van der Waals, elektrostatik, dan ikatan hidrogen—tanpa melibatkan pelarut atau panas. Ketelitian dalam mengendalikan parameter seperti kecepatan, tekanan udara, waktu proses, dan ukuran batch menjadi krusial dalam menjamin keberhasilan pembentukan FP.
Desain Eksperimen dan Refleksi Statistik
Peneliti menerapkan D-optimal design melalui perangkat lunak MODDE untuk menyusun 26 run eksperimental, termasuk 4 run replikasi untuk menilai kesalahan murni. Parameter bebas yang diuji meliputi:
-
Kecepatan (300–1500 rpm)
-
Waktu proses (15–60 menit)
-
Tekanan udara (0–40 psi)
-
Ukuran batch (6–20 g)
Empat CQA utama digunakan sebagai indikator performa sistem:
-
Kandungan homogen (Content Uniformity/RSD)
-
Laju disolusi ibuprofen
-
Ukuran partikel pada rentang X10 (PSA)
-
Intensitas spektrum FTIR pada pita C=O (1708 cm⁻¹)
Penilaian risiko menunjukkan bahwa keempat parameter proses tersebut berisiko menengah hingga tinggi terhadap CQAs, sehingga layak untuk dioptimalkan.
Temuan Eksperimental dan Interpretasi Konseptual
1. Pengaruh Ukuran Batch terhadap CQAs
Hasil menunjukkan bahwa batch size merupakan faktor paling signifikan dalam mempengaruhi laju disolusi, ukuran partikel, dan intensitas FTIR. Semakin besar batch, semakin cepat disolusi terjadi, semakin kecil ukuran partikel (menandakan kurangnya pelapisan), dan semakin tinggi intensitas FTIR (mengindikasikan lemahnya pembentukan ikatan hidrogen).
Interpretasi teoritis: Ukuran batch yang besar mengurangi efisiensi gaya gesek dalam sistem, menghambat de-aglomerasi partikel tamu dan distribusi yang seragam di atas partikel pembawa. Fenomena ini mendukung premis QbD bahwa pemahaman mekanisme proses sangat vital untuk mencapai atribut kualitas yang diinginkan.
2. Peran Kecepatan dan Interaksinya
Kecepatan (rpm) memiliki dampak negatif terhadap disolusi. Semakin tinggi kecepatannya, laju pelepasan ibuprofen justru menurun—indikator keberhasilan pembentukan FP. Namun, efek ini hanya optimal ketika ukuran batch rendah. Efek kuadratik dari kecepatan menunjukkan pola kurva cembung: peningkatan awal bermanfaat, tetapi setelah titik tertentu, terjadi efek attrition (pengelupasan partikel) akibat tumbukan berlebih.
Refleksi: Ini menunjukkan pentingnya mempertimbangkan non-linearitas dalam model prediktif farmasi dan kekuatan QbD dalam menavigasi hubungan kompleks semacam ini.
3. Validasi Ikatan Melalui FTIR
Penggunaan FTIR menjadi bukti tidak langsung keberhasilan pelapisan melalui deteksi ikatan hidrogen antara gugus karbonil (C=O) ibuprofen dan gugus hidroksil (OH) dari MCC. Intensitas pita 1708 cm⁻¹ menurun pada campuran yang dilapisi kering dibandingkan dengan campuran fisik.
Makna teoritis: Pendekatan ini memperluas konsep CQAs dari sekadar parameter fisik menjadi indikasi interaksi molekuler yang bersifat fungsional.
4. Homogenitas Campuran dan RSD
Variabilitas kandungan ibuprofen (RSD) dipengaruhi oleh berbagai interaksi: antara kecepatan dan batch size, waktu proses, serta tekanan udara. RSD optimal (<2%) tercapai saat kecepatan tinggi (≥800 rpm), batch kecil (≤10 g), dan waktu proses tidak terlalu lama.
Refleksi kritis: Ketepatan dalam mengidentifikasi RSD sebagai indikator keseragaman distribusi partikel aktif memperkuat posisi paper ini dalam menjembatani aspek desain formulasi dan pengendalian proses.
Visualisasi Desain Ruang Operasional (Design Space)
Penelitian ini secara cermat menyajikan peta “sweet spot” parameter proses (speed vs time) yang menghasilkan CQAs optimal: disolusi <85% dalam 60 menit dan RSD <5%. Dengan tekanan udara 40 psi dan batch size 6 g, diperoleh zona operasional dari 850–1500 rpm dan 15–60 menit proses.
Implikasi ilmiah: Ini mencerminkan penerapan prinsip QbD yang sesungguhnya—mengubah ruang kemungkinan menjadi ruang kendali (design space) yang dapat diprediksi dan direplikasi.
Kritik Terhadap Pendekatan Metodologis
1. Kelebihan
-
Penerapan QbD yang utuh dan sistematis
-
Validasi statistik ketat (R² ≥ 0.85 untuk semua respon)
-
Korelasi kuat antara data kuantitatif dan interpretasi molekuler (FTIR)
2. Keterbatasan
-
Rentang parameter tidak mencakup nilai ekstrem, sehingga desain ruang mungkin belum sepenuhnya generalisable.
-
Penggunaan satu model API (ibuprofen) membatasi generalisasi hasil ke sistem lain.
-
Penekanan pada peralatan prototipe yang dikembangkan internal, membuat replikasi eksternal menantang.
Usulan: Studi lanjutan dapat mencakup uji validasi pada batch produksi skala pilot, serta menggunakan bahan aktif dengan polaritas atau sifat kelarutan yang berbeda.
Kontribusi Ilmiah dan Potensi Aplikasi
Artikel ini memberikan kontribusi penting terhadap ilmu formulasi farmasi dengan:
-
Mendemonstrasikan efektivitas QbD sebagai pendekatan holistik dalam pengembangan proses.
-
Menunjukkan bahwa indikator non-tradisional seperti spektrum FTIR dapat menjadi metrik kualitas yang relevan.
-
Menyediakan model regresi prediktif yang mampu diadopsi dalam pengembangan produk sejenis.
Potensi aplikasi mencakup formulasi obat lepas lambat, pengurangan penggunaan pelarut (eco-friendly), dan peningkatan efisiensi produksi berbiaya rendah.
Kesimpulan
Penelitian ini tidak hanya menyajikan optimalisasi parameter, tetapi mengekspresikan filosofi QbD sebagai pendekatan epistemologis dalam pengembangan farmasi modern. Dengan memahami hubungan antara variabel proses dan atribut kualitas secara konseptual dan statistik, kita tidak hanya mengoptimalkan sistem, tetapi juga memperluas batas pengetahuan farmasi yang berbasis data dan kendali mutu.
📎 DOI Resmi Paper:
https://doi.org/10.1371/journal.pone.0206651
Jika Anda ingin versi Word atau PDF dari resensi ini, saya bisa bantu menyusunnya.
Teknik Kimia
Pemulihan Energi: Prinsip, Aplikasi, dan Dampak Lingkungan
Dipublikasikan oleh Raynata Sepia Listiawati pada 10 Februari 2025
Pemulihan energi
Pemulihan energi mencakup teknik atau metode apa pun untuk meminimalkan input energi ke sistem secara keseluruhan dengan pertukaran energi dari satu sub-sistem dari sistem keseluruhan dengan yang lain. Energi dapat dalam bentuk apa pun di kedua subsistem, tetapi sebagian besar sistem pemulihan energi menukar energi panas baik dalam bentuk yang nyata maupun laten.
Dalam beberapa situasi, penggunaan teknologi yang memungkinkan, baik penyimpanan energi panas harian atau penyimpanan energi panas musiman (STES, yang memungkinkan penyimpanan panas atau dingin di antara musim yang berlawanan), diperlukan agar pemulihan energi dapat dilakukan. Salah satu contohnya adalah limbah panas dari mesin pendingin udara yang disimpan dalam tangki penyangga untuk membantu pemanasan di malam hari.
Prinsip
Aplikasi umum dari prinsip ini adalah pada sistem yang memiliki aliran buangan atau aliran limbah yang ditransfer dari sistem ke sekitarnya. Beberapa energi dalam aliran material tersebut (sering kali berupa gas atau cairan) dapat ditransfer ke aliran material make-up atau input. Aliran massa masukan ini sering kali berasal dari lingkungan sistem, yang berada pada kondisi sekitar, berada pada suhu yang lebih rendah daripada aliran limbah. Perbedaan suhu ini memungkinkan terjadinya perpindahan panas dan dengan demikian perpindahan energi, atau dalam hal ini, pemulihan. Energi panas sering kali dipulihkan dari aliran limbah cair atau gas ke udara segar dan asupan air di dalam gedung, seperti untuk sistem HVAC, atau sistem proses.
Pendekatan sistem
Konsumsi energi adalah bagian penting dari sebagian besar aktivitas manusia. Konsumsi ini melibatkan konversi satu sistem energi ke sistem energi lainnya, misalnya: Konversi energi mekanik ke energi listrik, yang kemudian dapat menyalakan komputer, lampu, motor, dll. Energi input menggerakkan pekerjaan dan sebagian besar diubah menjadi panas atau mengikuti produk dalam proses sebagai energi output. Sistem pemulihan energi memanen daya output dan menyediakannya sebagai daya input untuk proses yang sama atau proses lainnya.
Sistem pemulihan energi akan menutup siklus energi ini untuk mencegah daya input dilepaskan kembali ke alam dan lebih baik digunakan dalam bentuk lain dari pekerjaan yang diinginkan.
Contoh
Pemulihan panas diimplementasikan pada sumber panas seperti misalnya pabrik baja. Air pendingin yang dipanaskan dari proses tersebut dijual untuk memanaskan rumah, toko, dan kantor di daerah sekitarnya.
- Pengereman regeneratif digunakan pada mobil listrik, kereta api, derek berat, dll. Di mana energi yang dikonsumsi saat menaikkan potensi dikembalikan ke pemasok listrik saat dilepaskan.
- Sistem pengurangan tekanan aktif di mana tekanan diferensial dalam aliran fluida bertekanan dipulihkan daripada diubah menjadi panas dalam katup pengurangan tekanan dan dilepaskan.
- Ventilasi pemulihan energi
- Daur ulang energi
- Daur ulang panas air
- Ventilasi pemulihan panas
- Pembangkit uap pemulihan panas
- Mesin Pembangkit Panas Limbah Siklon
- Generator turboexpander hidrogen
- Dioda termal
- Pengoksidasi termal
- Modul Termoelektrik
- Unit pemulihan panas limbah
Senyawa Turbo Listrik (ETC)
Electric Turbo Compounding (ETC) adalah solusi teknologi untuk tantangan meningkatkan efisiensi bahan bakar mesin gas dan diesel dengan memulihkan energi limbah dari gas buang.
STES
- Di sebuah pengecoran logam di Swedia, limbah panas dipulihkan dan disimpan dalam massa besar batuan dasar asli yang ditembus oleh sekelompok 140 lubang bor yang dilengkapi dengan penukar panas (diameter 155mm) sedalam 150m. Penyimpanan ini digunakan untuk memanaskan pabrik yang berdekatan sesuai kebutuhan, bahkan berbulan-bulan kemudian.
- Komunitas Tenaga Surya Drake Landing di Alberta, Kanada menggunakan STES untuk memulihkan dan memanfaatkan panas alami yang akan terbuang percuma. Komunitas ini menggunakan sekelompok sumur bor di batuan dasar untuk penyimpanan panas antar musim, dan ini memungkinkan untuk mendapatkan 97 persen pemanas ruangan sepanjang tahun dari kolektor panas matahari di atap garasi.
- Suhu musim dingin dapat dipulihkan dengan mengedarkan air melalui menara pendingin kering dan menggunakannya untuk mendinginkan akuifer dalam atau kelompok lubang bor. Suhu dingin ini kemudian dipulihkan dari penyimpanan untuk AC musim panas. Dengan koefisien kinerja (COP) 20 hingga 40, metode pendinginan ini bisa sepuluh kali lebih efisien daripada AC konvensional.
Dampak lingkungan
Ada potensi besar untuk pemulihan energi dalam sistem yang ringkas seperti industri besar dan utilitas. Bersama dengan konservasi energi, seharusnya dapat mengurangi konsumsi energi dunia secara dramatis. Efek dari hal ini adalah:
- Berkurangnya jumlah pembangkit listrik tenaga batu bara
- Berkurangnya partikel di udara, NOx dan CO2 - peningkatan kualitas udara
- Memperlambat atau mengurangi perubahan iklim
- Tagihan bahan bakar yang lebih rendah untuk transportasi
- Ketersediaan minyak mentah yang lebih lama
- Perubahan industri dan ekonomi yang belum sepenuhnya diteliti
Pada tahun 2008, Tom Casten, ketua Pengembangan Energi Daur Ulang, mengatakan bahwa "Kami pikir kami dapat menghasilkan sekitar 19 hingga 20 persen listrik AS dengan panas yang saat ini dibuang oleh industri."
Sebuah studi Departemen Energi tahun 2007 menemukan potensi 135.000 megawatt gabungan panas dan listrik (yang menggunakan pemulihan energi) di AS, dan studi Lawrence Berkley National Laboratory mengidentifikasi sekitar 64.000 megawatt yang dapat diperoleh dari energi limbah industri, tidak termasuk CHP. Studi-studi ini menunjukkan bahwa sekitar 200.000 megawatt, atau 20%, dari total kapasitas listrik dapat berasal dari daur ulang energi di AS. Penggunaan daur ulang energi secara luas dapat mengurangi emisi pemanasan global sekitar 20%. Memang, pada tahun 2005, sekitar 42% polusi gas rumah kaca di AS berasal dari produksi listrik dan 27% dari produksi panas.
Sulit untuk mengukur dampak lingkungan dari implementasi pemulihan energi global di beberapa sektor. Hambatan utamanya adalah:
- Kurangnya teknologi yang efisien untuk rumah-rumah pribadi. Sistem pemulihan panas di rumah-rumah pribadi dapat memiliki efisiensi serendah 30% atau kurang. Mungkin lebih realistis untuk menggunakan konservasi energi seperti insulasi termal atau bangunan yang lebih baik. Banyak daerah yang lebih bergantung pada pendinginan paksa dan sistem untuk mengekstraksi panas dari tempat tinggal untuk digunakan untuk keperluan lain tidak tersedia secara luas.
- Infrastruktur yang tidak efektif. Pemulihan panas khususnya membutuhkan jarak yang pendek dari produsen ke konsumen agar dapat berjalan. Solusinya adalah memindahkan konsumen besar ke sekitar produsen. Hal ini dapat menimbulkan komplikasi lainnya.
- Sektor transportasi belum siap. Dengan sektor transportasi yang menggunakan sekitar 20% dari pasokan energi, sebagian besar energi dihabiskan untuk mengatasi gravitasi dan gesekan. Mobil listrik dengan pengereman regeneratif tampaknya menjadi kandidat terbaik untuk pemulihan energi. Sistem angin pada kapal sedang dalam pengembangan. Sangat sedikit pekerjaan pada industri penerbangan yang diketahui di bidang ini.
Disadur dari: en.wikipedia.org
Teknik Kimia
Merancang Proses Kimia: Pendekatan, Dokumentasi, dan Pertimbangan
Dipublikasikan oleh Raynata Sepia Listiawati pada 10 Februari 2025
Desain proses
Dalam teknik kimia, desain proses adalah pemilihan dan pengurutan unit untuk transformasi fisik dan/atau kimiawi bahan yang diinginkan. Desain proses adalah pusat dari teknik kimia, dan dapat dianggap sebagai puncak dari bidang tersebut, yang menyatukan semua komponen bidang tersebut.
Desain proses dapat berupa desain fasilitas baru atau dapat berupa modifikasi atau perluasan fasilitas yang sudah ada. Desain dimulai dari tingkat konseptual dan pada akhirnya berakhir dalam bentuk rencana fabrikasi dan konstruksi.Desain proses berbeda dengan desain peralatan, yang lebih dekat dengan desain operasi unit. Proses sering kali mencakup banyak operasi unit.
Dokumentasi
Dokumen desain proses berfungsi untuk mendefinisikan desain dan memastikan bahwa komponen desain saling cocok. Dokumen ini berguna dalam mengkomunikasikan ide dan rencana kepada insinyur lain yang terlibat dalam desain, kepada badan pengatur eksternal, vendor peralatan, dan kontraktor konstruksi.
Dalam urutan yang semakin rinci, dokumen desain proses meliputi:
- Diagram aliran blok (BFD): Diagram yang sangat sederhana yang terdiri dari persegi panjang dan garis yang menunjukkan aliran material atau energi utama.
- Diagram aliran proses (PFD): Biasanya merupakan diagram yang lebih kompleks dari operasi unit utama serta garis aliran. Diagram ini biasanya mencakup neraca material, dan terkadang neraca energi, yang menunjukkan laju aliran tipikal atau desain, komposisi aliran, serta tekanan dan suhu aliran dan peralatan. Ini adalah dokumen utama dalam desain proses.
- Diagram perpipaan dan instrumentasi (P&ID): Diagram yang menunjukkan setiap pipa dengan kelas pipa (baja karbon atau baja tahan karat) dan ukuran pipa (diameter). Diagram ini juga menunjukkan katup beserta lokasi instrumen dan skema kontrol proses.
- Spesifikasi: Persyaratan desain tertulis dari semua item peralatan utama.
Perancang proses biasanya menulis manual operasi tentang cara memulai, mengoperasikan, dan mematikan proses. Mereka juga sering mengembangkan rencana kecelakaan dan proyeksi operasi proses terhadap lingkungan.
Dokumen-dokumen tersebut disimpan setelah pembangunan fasilitas proses untuk menjadi acuan bagi personel yang mengoperasikan. Dokumen-dokumen tersebut juga berguna ketika ada modifikasi pada fasilitas yang direncanakan. Metode utama untuk mengembangkan dokumen proses adalah diagram alir proses.
Pertimbangan desain
Ada beberapa pertimbangan yang perlu dibuat saat merancang unit proses kimia. Konseptualisasi dan pertimbangan desain dapat dimulai setelah kemurnian produk, hasil, dan laju produksi ditentukan.
Tujuan yang mungkin ingin dimasukkan dalam desain:
- Laju keluaran
- Hasil proses
- Kemurnian produk
Batasan-batasan meliputi:
- Biaya modal
- Ruang yang tersedia
Masalah keamanan: pertimbangan terhadap analisis risiko kecelakaan industri atau bahan kimia berbahaya.
- Dampak lingkungan dan proyeksi limbah dan emisi
- Produksi/daur ulang limbah
- Biaya operasional dan pemeliharaan
Faktor-faktor lain yang dapat disertakan oleh perancang adalah:
- Keandalan
- Redundansi
- Fleksibilitas
- Variabilitas
Sumber informasi desain
Desainer biasanya tidak memulai dari awal, terutama untuk proyek yang kompleks. Seringkali para insinyur memiliki data pabrik percontohan yang tersedia atau data dari fasilitas operasi skala penuh. Sumber informasi lain termasuk kriteria desain eksklusif yang disediakan oleh pemberi lisensi proses, data ilmiah yang dipublikasikan, eksperimen laboratorium, dan pemasok bahan baku dan utilitas.
Proses desain
Desain dimulai dengan sintesis proses - pilihan teknologi dan kombinasi unit industri untuk mencapai tujuan. Desain yang lebih rinci berlanjut ketika insinyur dan pemangku kepentingan lainnya menandatangani setiap tahap: konseptual hingga desain terperinci.
Perangkat lunak simulasi sering digunakan oleh para insinyur desain. Simulasi dapat mengidentifikasi kelemahan dalam desain dan memungkinkan para insinyur memilih alternatif yang lebih baik. Namun, para insinyur masih mengandalkan heuristik, intuisi, dan pengalaman saat merancang suatu proses. Kreativitas manusia adalah elemen dalam desain yang kompleks.
Disadur dari: en.wikipedia.org
Teknik Kimia
Diagram Alir Proses dalam Teknik Kimia: Konsep, Komponen, dan Contoh
Dipublikasikan oleh Raynata Sepia Listiawati pada 10 Februari 2025
Diagram alir proses
Diagram alir proses (PFD) adalah diagram yang biasa digunakan dalam teknik kimia dan proses untuk menunjukkan aliran umum proses dan peralatan pabrik. PFD menampilkan hubungan antara peralatan utama dari fasilitas pabrik dan tidak menunjukkan detail kecil seperti detail perpipaan dan peruntukan. Istilah lain yang umum digunakan untuk PFD adalah diagram alir proses. Ini adalah dokumen utama dalam desain proses.
Konten khas dari diagram alir proses
Biasanya, diagram alir proses dari satu unit proses meliputi yang berikut ini:
- Pemipaan proses
- Item peralatan utama
- Koneksi dengan sistem lain
- Aliran pintas dan resirkulasi (daur ulang) utama
- Data operasional
- Nama aliran proses
Diagram aliran proses umumnya tidak menyertakan:
- Kelas pipa atau nomor jalur perpipaan
- Detail instrumentasi
- Jalur pintas kecil
- Instrumentasi
- Pengontrol seperti Kontrol Level atau Kontrol Aliran
- Katup isolasi dan penutup
- Ventilasi dan saluran pembuangan perawatan
Contoh diagram aliran proses
Diagram alir proses di bawah ini menggambarkan satu proses unit teknik kimia yang dikenal sebagai pabrik pengolahan amina:
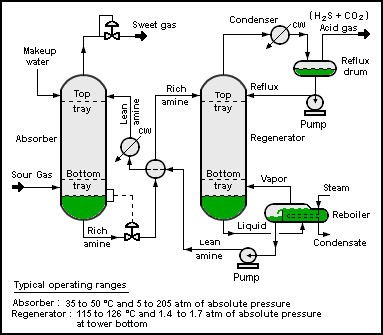
Beberapa unit proses dalam pabrik industri
Diagram alir proses di bawah ini adalah contoh diagram alir skematik atau diagram alir blok dan menggambarkan berbagai unit proses dalam kilang minyak biasa:
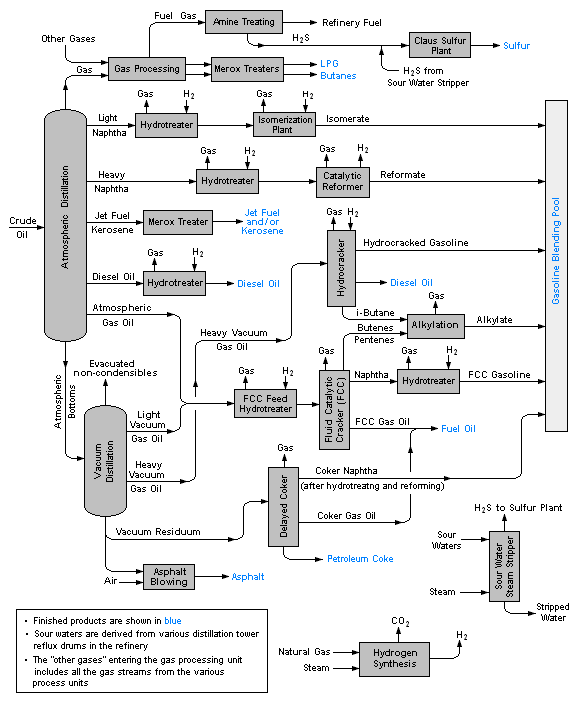
Hal-hal lain yang menarik
PFD dapat dibuat dengan komputer dari simulator proses (lihat Daftar Simulator Proses Kimia), paket CAD, atau perangkat lunak diagram alir dengan menggunakan perpustakaan simbol teknik kimia. Aturan dan simbol tersedia dari organisasi standardisasi seperti DIN, ISO atau ANSI. Seringkali PFD diproduksi di atas lembaran kertas berukuran besar.
PFD dari banyak proses komersial dapat ditemukan dalam literatur, khususnya dalam ensiklopedia teknologi kimia, meskipun beberapa di antaranya mungkin sudah ketinggalan zaman. Untuk menemukan yang terbaru, basis data paten seperti yang tersedia dari Kantor Paten dan Merek Dagang Amerika Serikat dapat berguna.
Standar
- ISO 15519-1: 2010 (en): Spesifikasi diagram untuk industri proses - Bagian 1: Aturan umum
- ISO 15519-2:2015 (en): Spesifikasi diagram untuk industri proses - Bagian 2: Pengukuran dan kontrol
- ISO 10628-1:2014 (en): Diagram untuk industri kimia dan petrokimia - Bagian 1: Spesifikasi diagram
- ISO 10628-2:2012 (en): Diagram untuk industri kimia dan petrokimia - Bagian 2: Simbol grafis
- ANSI Y32.11: Simbol Grafis Untuk Diagram Aliran Proses (ditarik pada tahun 2003)
- SAA AS 1109: Simbol Grafis Untuk Diagram Alir Proses Untuk Industri Makanan
Disadur dari: en.wikipedia.org
Teknik Kimia
Pengendalian Proses: Pengertian, Contoh, dan Tipe Proses
Dipublikasikan oleh Raynata Sepia Listiawati pada 10 Februari 2025
Pengendalian proses
Pengendalian proses adalah disiplin rekayasa yang melibatkan mekanisme dan algoritme untuk mengendalikan keluaran dari suatu proses dengan hasil yang diinginkan. Contohnya, temperatur reaktor kimia harus dikendalikan untuk menjaga keluaran produk.
Pengendalian proses banyak sekali digunakan pada industri dan menjaga konsistensi produk produksi massal seperti proses pada pengilangan minyak, pembuatan kertas, bahan kimia, pembangkit listrik, dan lainnya. Pengendalian proses mengutamakan otomasi sehingga hanya diperlukan sedikit personel untuk mengoperasikan proses yang kompleks.
Sebagai contoh adalah sistem pengaturan temperatur ruangan agar temperatur ruangan terjaga konstan setiap saat, misalnya pada 20 °C. Pada kasus ini, temperatur disebut sebagai variabel terkendali. Selain itu, karena temperatur diukur oleh suatu termometer dan digunakan untuk menentukan kerja pengendali (apakah ruangan perlu didinginkan atau tidak), temperatur juga merupakan variabel input. Temperatur yang diinginkan (20 °C) adalah setpoint. Keadaan dari pendingin (misalnya laju keluaran udara pendingin) dinamakan variabel termanipulasi karena merupakan variabel yang terkena aksi pengendalian.
Alat pengendalian yang umum digunakan adalah Programmable Logic Controller (PLC). Alat ini digunakan untuk membaca input analog maupun digital, melakukan serangkaian program logika, dan menghasilkan serangkaian output analog maupun digital. Pada kasus sistem pengaturan temperatur, temperatur ruangan menjadi input bagi PLC.
Pernyataan-pernyataan logis akan membandingkan setpoint dengan masukan nilai temperatur dan menentukan apakah perlu dilakukan penambahan atau pengurangan pendinginan untuk menjaga temperatur agar tetap konstan. Output dari PLC akan memperbesar atau memperkecil aliran keluaran udara pendingin bergantung pada kebutuhan. Untuk suatu sistem pengendalian yang kompleks, perlu digunakan sistem pengendalian yang lebih kompleks daripada PLC. Contoh dari sistem ini adalah Distributed Control System (DCS) atau sistem SCADA.
Tipe proses
Dalam praktiknya, sistem pengendalian proses dapat dikarakteristikkan dalam bentuk:
- Diskrit – Terdapat pada aplikasi manufaktur dan pengemasan. Pemasangan dengan bantuan robot, seperti yang umum digunakan pada produksi otomotif, dapat dikarakteristikkan sebagai pengendalian proses diskrit. Sebagian besar proses manufaktur diskrit melibatkan produksi bagian produk secara diskrit, seperti pembentukan logam.
- Partaian – Beberapa aplikasi membutuhkan digabungkannya beberapa bahan baku spesifik dengan cara tertentu pada jangka waktu tertentu untuk menghasilkan produk samping atau produk akhir. Contohnya adalah pada produksi lem dan perekat, yang umumnya membutuhkan pencampuran bahan baku dalam suatu reaktor yang dipanaskan selama periode waktu tertentu. Contoh lain adalah pada produksi makanan dan obat. Proses partaian biasanya dilakukan untuk memproduksi produk dengan kapasitas rendah hingga sedang.
- Kontinu – Seringkali proses produksi berlangsung secara terus menerus tanpa terhenti. Pengendalian temperatur air pada jaket pemanas secara terus menerus adalah contoh pengendalian proses secara kontinu. Contoh produksi yang berlangsung secara kontinu adalah produksi bahan bakar. Proses kontinu pada proses produksi digunakan untuk memproduksi produk dengan kapasitas besar.
Sumber: id.wikipedia.org